氯化物是引发铁质文物腐蚀,导致铁质文物不稳定的重要原因之一。确定氯化物的种类和性质,进而选择有效的方法进行控制、脱氯或转化处理,是铁质文物保护过程中的关键。四方纤铁矿(β-FeOOH)的晶体结构中可容纳氯离子,是铁质文物腐蚀产物中最常见的含氯腐蚀产物。
1977年,在意大利Pianetto Forli的高卢墓葬出土的铁矛头、铁斧上发现β-FeOOH,这是文献记载的首次在铁质文物上发现β-FeOOH。该铁器上存在“活性腐蚀区域”,在相对湿度较高的环境中该区域能不断产生新鲜的腐蚀产物。比较活性区域和非活性区域的腐蚀产物发现,活性区域含有β-FeOOH,而非活性区域没有,因此β-FeOOH能够促进铁质文物的腐蚀,其晶体具有隧道结构,隧道中含有Cl-,被释放出来对铁质文物造成腐蚀。

(a) 9个晶胞
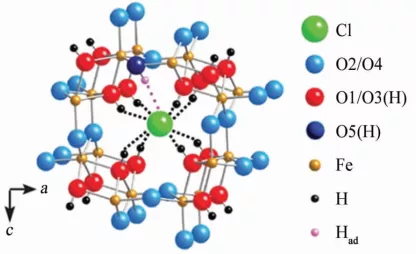
(b) 隧道结构
图1 β-FeOOH的晶体结构
自此之后,人们开始研究β-FeOOH在铁质文物腐蚀过程中的角色及其处理对策。
大多数学者认为β-FeOOH是一种对铁质文物危害极大的腐蚀产物,是活性腐蚀的主要特征之一,是铁器出土后迅速损坏的主要原因,其生成过程与青铜器上发生的“青铜病”极为类似。学者们称其为铁质文物的“有害锈”、腐蚀的“催化剂”、Cl-的“储蓄器”等。
但也有学者对此有不同认识。STAHL等认为β-FeOOH只是铁质文物在氯化物含量高的环境中的腐蚀特征,是腐蚀的结果而不是原因,其本身不会对铁质文物构成威胁。
造成这种分歧的主要原因是不同方法、不同环境中产生的β-FeOOH,Cl-含量差别很大,而Cl-的存在形式也有明显区别。文献记载β-FeOOH中的Cl-质量分数从0.87%~17%不等。β-FeOOH的晶体内部隧道结构中有Cl-,而晶体表面通常也吸附Cl-。近年来同步辐射分析技术的应用证明了这两种Cl-的存在与区别。因此,要进一步了解β-FeOOH对铁质文物的危害,应当区分两种不同的Cl-,分别研究其在腐蚀中的作用,进而提出相应的处理方法。
近年来,在沧州铁狮子等室外铁器,天津、厦门、蓬莱、绥中、黄骅、海南、宁波、华光礁I号沉船等地海洋出水铁器以及陕西、自贡、河南、深圳、济南、广西等地出土铁器的腐蚀产物中均发现了β-FeOOH。因此,了解β-FeOOH的产生过程及其对铁质文物的危害,并进一步研究其腐蚀控制或转化处理的方法,对我国的铁质文物保护具有重要意义。
β-FeOOH在铁质文物腐蚀中的生成过程
β-FeOOH是海洋出水铁器的主要腐蚀产物之一,在出土铁器上也常有发现。它不是铁器最初的腐蚀产物,而是在铁器出土、出水接触空气后才大量生成的。铁器上能够转化成β-FeOOH的腐蚀产物有FeCl2?FeCl3?FeOCl?Fe2(OH)3Cl、绿锈等。
在铁质文物腐蚀过程中,β-FeOOH的生成途径如图2所示。它可由FeCl2水解氧化生成(过程中可能有中间产物FeCl3?FeOCl),也可由Fe2(OH)3Cl氧化生成(过程中可能有中间产物绿锈),其生成环境中需有较高含量的Cl-和Fe2+,因此通常在铁器点腐蚀、缝隙腐蚀区域生成。
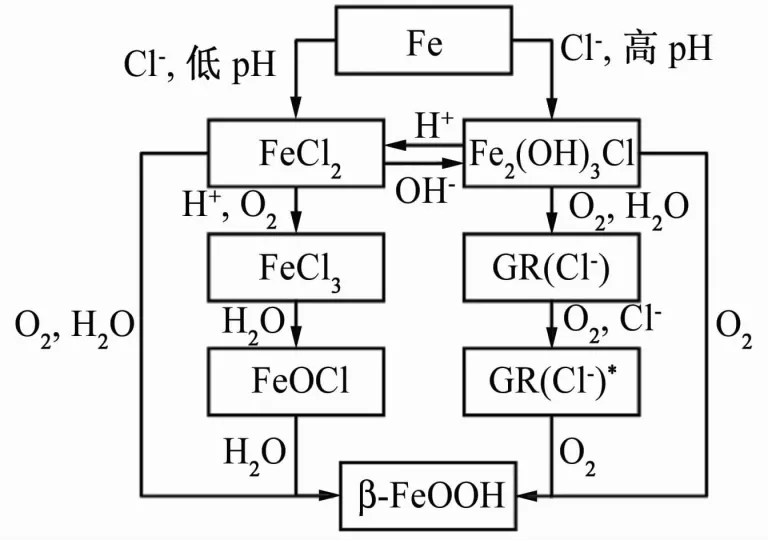
图2 β-FeOOH在铁质文物腐蚀中的生成途径
β-FeOOH对铁质文物的危害
Cl-是促进铁质文物腐蚀,导致其损坏的重要因素。作为铁质文物出土出水后的主要含氯腐蚀产物,β-FeOOH通常被认为是一种对铁质文物危害极大的有害锈。其对铁质文物产生危害的主要原因在于β-FeOOH晶体的生长,β-FeOOH作为反应物参与腐蚀过程,以及β-FeOOH中的Cl-。β-FeOOH表面吸附的Cl-和晶体隧道结构中的Cl-在腐蚀中的作用有明显区别,因此有必要分开讨论。
β-FeOOH晶体的生长
β-FeOOH晶体通常为细长针状结构,密度较低。1mol β-FeOOH的体积约为25cm3,这大约是1mol金属铁的3倍,因此其生长过程也是体积剧烈膨胀的过程。出土铁器中的FeCl2以溶液形式存在于锈层孔洞、缝隙中,当接触空气后迅速氧化水解产生β-FeOOH,给锈层造成压力,导致锈层出现层状剥离、裂缝甚至断裂。这是铁器出土后迅速损坏的主要原因。
THICKETT调研了284件铁质文物的损坏原因,发现其中78%的主要损坏原因是β-FeOOH生长;PINGITORE等对克罗托内国家考古博物馆20年前修复的一批铁质文物进行调研,结果发现β-FeOOH往往在铁基体与锈层中间产生,这导致了铁质文物在修复后仍然会快速损坏。
β-FeOOH作为反应物参与腐蚀过程
在潮湿的大气环境中,β-FeOOH在腐蚀过程中可以作为阴极去极化剂,接受电子并和Fe2+反应生成Fe3O4。在缺氧环境中,β-FeOOH也会直接与Fe2+反应生成Fe3O4。其反应机制为溶解-再结晶。在α?β?γ三种FeOOH中,β-FeOOH溶解度最大,发生此反应的转化率也最高,经常在铁质文物腐蚀过程中发生,这是含氯环境中Fe3O4在铁质文物的锈蚀产物中含量高的原因之一。
β-FeOOH晶体表面吸附的Cl-
ZUCCHI等早在1977年首次在铁质文物上发现β-FeOOH时就提出,β-FeOOH释放出Cl-是铁器加速腐蚀的原因,GILBERG等也持此观点,但他们并没有区分β-FeOOH晶体表面吸附的Cl-和隧道结构中的Cl-。近年来的研究表明,晶体表面吸附的Cl-才是促进出土、出水铁质文物腐蚀的主要原因。
β-FeOOH晶体表面除吸附Cl-外,也会吸附H+,从而使表面部分质子化。β-FeOOH表面吸附的Cl-对铁质文物的危害主要有:
HCl作为强酸,可造成铁锈层的局部溶解,使其强度下降,裂缝增大,且同等pH下,HCl比其他酸更容易溶解铁锈。
HCl会直接腐蚀铁基体,Cl-在反应过程中实际起到催化剂的作用,HCl不断消耗又不断重新生成,因此这一过程被称为“酸再生循环”过程。这一过程也是铁质文物出土、出水后损坏的原因,如果不对其进行干预,可持续发生直至铁器损毁。
β-FeOOH具有明显的吸湿性,可降低腐蚀发生所需的相对湿度。水分子通过氢键和弱电荷转移作用吸附在晶体表面。
WATKINSON等发现,β-FeOOH的吸湿性与表面Cl-有关,未清洗的β-FeOOH即使在低湿度下也有明显的吸湿性,使表面形成富含HCl的电解质溶液,15%的RH就可造成铁粉腐蚀,RH在20%以上时则腐蚀明显加速,且同等RH下,β-FeOOH比FeCl2对铁粉腐蚀的促进作用更明显。只有将RH降至12%以下,腐蚀才不会发生。
THICKETT等进一步研究发现,β-FeOOH生成时湿度越高,其对腐蚀的促进越明显。例如,β-FeOOH在RH为80%条件下生成,其与铁粉、FeCl2混合后,即使将RH降低至13%,铁粉依然会发生腐蚀。
HCl具有挥发性,可能会对附近的其他金属器造成腐蚀。WATKINSON等在试验时偶然发现,和β-FeOOH样品处于同一密闭空间内但未与其接触的不锈钢药匙和铝箔均发生了腐蚀,并生成含氯产物,他们认为这是β-FeOOH表面HCl挥发造成的。
β-FeOOH晶体隧道结构中的Cl-
相比晶体表面吸附的Cl-,隧道结构中的Cl-难以移动和释放。因此很多学者认为,它不会促进铁质文物的进一步腐蚀。随着β-FeOOH的生成,游离的Cl-进入隧道结构,铁质文物的腐蚀速率下降,最终达到基本稳定,即腐蚀速率很低的状态。虽然,对铁质文物进行脱氯处理难以将β-FeOOH隧道结构中的Cl-全部脱除,但残余Cl-也不会造成危害。
WATKINSON等发现,在RH为80%条件下,自制β-FeOOH使铁粉发生明显腐蚀;而将β-FeOOH用水清洗后,其成分仍为纯β-FeOOH,且含有2.0%~2.5%的Cl-,但其吸水性明显减弱,铁粉的腐蚀速率也明显降低,腐蚀接近停止。
如果β-FeOOH转化为其他晶型(如α-FeOOH),则其隧道结构中的Cl-会被释放,促进铁器腐蚀。
GILBERG等认为相对于α-FeOOH,β-FeOOH是亚稳定的,容易转化。
COOK等发现,在海洋大气环境中,短期暴露钢片表面有β-FeOOH,长期暴露钢片表面却没有,这是因为在长期暴露过程中β-FeOOH发生了转化。
但WATKINSON等经过试验发现,在密封玻璃瓶中保存23年后,纯β-FeOOH样品的成分未发生变化。
环境中的酸性污染气体也会促进β-FeOOH的溶解。THICKETT等通过调研和试验发现,合成的β-FeOOH和铁质文物样品上的β-FeOOH都会缓慢的转化为α-FeOOH,湿度越高转化越快,而乙酸对转化有明显的促进作用。当β-FeOOH转化为α-FeOOH时,β-FeOOH隧道结构中的Cl-被释放出来,促进腐蚀,影响铁器的长期稳定性。
在高温下,β-FeOOH会脱水转化为α-Fe2O3,同时释放出HCl。STAHL等认为该反应在200℃以下不会发生。THICKETT在一个38年前从铁器上取下的β-FeOOH样品上发现了β-FeOOH向α-Fe2O3的转变,并认为常温下该反应也会发生,虽然反应缓慢,但不可忽略。
结语
β-FeOOH是铁质文物腐蚀损坏过程中的关键腐蚀产物。它既是铁质文物在(局部)高含量氯化物作用下的结果,又是造成铁质文物进一步持续腐蚀的原因。β-FeOOH往往在铁质文物出土、出水后由FeCl2?Fe2(OH)3Cl等中间产物氧化水解生成,其过程与青铜器表面发生的“青铜病”类似,对铁质文物造成物理、化学两方面的损害。
β-FeOOH的晶体表面和隧道结构中都有Cl-(HCl)。晶体表面吸附的Cl-会直接促进铁质文物腐蚀,并使腐蚀循环发生;虽然隧道结构中的Cl-相对稳定,不会直接参与腐蚀过程,但也难以脱除,在环境因素影响下β-FeOOH转变为其他物相而被释放,从而促进腐蚀,因此在铁质文物的长期保存过程中仍是隐患。
因此,对含有β-FeOOH的铁质文物进行有针对性的保护处理,是铁质文物保护中的关键步骤,也是铁质文物保护研究中的关键问题。目前主要有两种思路:
一是预防性保护,即通过控制温度、相对湿度、氧气含量等环境因素阻止β-FeOOH的产生,并阻止已生成的β-FeOOH对铁质文物的腐蚀。
二是干预性保护,即脱除β-FeOOH中的氯离子,甚至将其转化为其他物相,以消除其对铁质文物的威胁。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





