摘要
采用动电位极化技术、慢应变速率拉伸实验 (SSRT) 以及扫描电子显微镜 (SEM) 等方法研究了硫酸盐还原菌 (SRB) 新陈代谢对2205双相不锈钢 (DSS) 在3.5% (质量分数) NaCl溶液中的应力腐蚀开裂 (SCC) 行为的影响。结果表明,与无菌溶液中相比,SRB的存在促进了2205DSS的阳极溶解过程,诱发了点蚀,为SCC萌生提供了裂纹源。2205DSS的SCC敏感性与SRB活性浓度呈正相关,在稳定生长期SRB活性浓度最大,此时2205DSS的SCC敏感性最大。2205DSS在含SRB的3.5%NaCl溶液中发生的SCC机理为阳极溶解和氢脆混合控制机制。SRB作用下,2205DSS中铁素体相表现为穿晶解理特征,奥氏体相表现为韧性撕裂的特征,铁素体相具有更高的SCC敏感性。
关键词: 2205双相不锈钢 ; 硫酸盐还原菌 ; 微生物腐蚀 ; 应力腐蚀开裂\
近年来,海洋经济已成为国家经济的重要增长点,国家对海洋资源的开发利用正不断增长。发展海洋装备,建设海洋工程是推进和实施国家海洋战略的重要内容。2205 DSS因具有奥氏体相 (γ) 和铁素体相 (α) 组织,且两相比例适宜,其兼有奥氏体不锈钢的优良焊接性和韧性与铁素体不锈钢的较高强度和耐氯化物应力腐蚀性能[1-3],进而逐渐取代316L及904L等奥氏体不锈钢应用于海洋结构钢、海底管道等设备上[4,5]。海洋环境具有多元性、复杂性和可变性特点,这使材料的腐蚀问题复杂化。加之载荷及洋流等冲击,因而材料在海水中服役极易发生应力腐蚀开裂 (SCC)。
目前,大部分学者对双相不锈钢在海洋中SCC行为的研究主要集中在氯化物SCC。林红先等[6]对22CrDSS与304L、316L钢在氯化物溶液中的SCC性能进行了比较,其结果表明22CrDSS在氯化物环境中具有更好的耐SCC性能。Tsai等[7]研究了2205DSS在26% (质量分数) NaCl溶液中90 ℃时不同电位下的SCC敏感性,结果表明,在电位小于-160 mV (SCE) 时,2205 DSS对SCC无敏感性;在电位大于-160 mV (SCE) 时,SCC敏感性随电位增加而增加,且SCC的扩展是由点蚀诱发铁素体α相优先选择性溶解的过程。Wu等[8]研究了海洋大气环境下2205DSS在不同pH和充氢电流密度下的电化学和SCC行为,结果表明,2205DSS的耐点蚀性能随pH的降低而降低,对SCC的敏感性随pH的降低或充氢电流密度的增大而提高。
实际上,海洋中的服役材料处于复杂的环境中,不仅受到Cl-和应力的影响,还在很大程度上受到海洋中微生物的影响[9],三者的协同作用与钢体的SCC程度密切相关。微生物腐蚀 (MIC) 是破坏最严重的腐蚀形式之一[10-13]。在生产现场已经发生细菌导致的裂纹开裂[14-16]。有学者通过电化学调频[17]和慢应变速率拉伸实验 (SSRT) 也证实了微生物会辅助SCC的发生[18-20]。但目前关于海洋中应力与微生物同时作用下SCC研究还很少。Wu等[21-23]对应力作用下管线钢的微生物腐蚀行为进行了系统的研究,结果表明SRB的活性导致点蚀萌生,外加弹性应力促进了点蚀的生长;SRB和浅层应力对管线钢氢通量有协同促进作用。Javaherdashti等[18]采用慢应变率实验研究了在人工合成海水环境 (3.5% (质量分数) NaCl) 中含SRB纯菌和混合菌对碳钢SCC行为的影响。结果表明:在有菌介质中SCC敏感性较高。在无菌介质中试样呈韧性断裂;而在有菌介质中SRB促进了H扩散到金属中,试样具有脆性开裂特征。Huang[24]在有/无SRB的海泥中不同电位下对API5LX52钢进行了SSRT和氢渗透实验。结果表明,SRB对环境敏感断裂的影响可能是SRB加速腐蚀速率和H进入金属的结果。另外,一些失效分析表明[18,25],在一定使用条件下,微生物的存在可以极大地改变腐蚀环境的性质,从而对局部腐蚀 (如点蚀)、SCC等产生重大影响。然而,关于海洋中2205DSS在SRB作用下SCC的研究鲜有报道,因而研究SRB等微生物在海洋环境中对2205DSS的SCC行为的影响具有重要的理论和实际意义。
本研究采用电化学和SSRT实验研究SRB新陈代谢对2205DSS在3.5%NaCl溶液中的SCC行为的影响,通过计算断面收缩率和延伸率评估SRB新陈代谢对2205DSS在海水中SCC敏感性的影响。采用扫描电镜 (SEM) 对断口形貌进行分析,探究SRB作用下2205DSS断裂机制,为提高2205DSS在海洋环境中的应用提供理论支撑。
1 实验方法
1.1 实验材料
本研究选用的材料为2205DSS,其主要化学成分 (质量分数,%) 为:C 0.02,N 0.16,Si 0.68,Mn 1.2,Cr 22,Ni 5.42,Mo 3.03,S 0.002,P 0.018,Fe 余量。将其制成尺寸为10 mm×10 mm×2 mm的金相试样,依次用水砂纸从80#打磨至2000#,用人造金刚石研磨膏机械抛光至2.5µm,经王水 (37%浓盐酸与67%浓硝酸按体积比3∶1混合) 浸蚀后,在金相显微镜 (LEICA DMI 5000 M) 上得到2205DSS的金相显微镜组织见图1。2205DSS的组织在室温下为铁素体+奥氏体的双相组织,二者比例适当。其中,深色区域为α铁素体,浅色区域为γ奥氏体。

图1 2205DSS的金相显微组织
线切割SSRT试样尺寸如图2所示。实验前将试样编号并用水砂纸将试样测试区域表面从80#沿同一方向轴向打磨至2000#,然后依次用丙酮、去离子水清洗并用冷风吹干后放入干燥器干燥,之后测量标记出试样拉伸部位,记录拉伸区域的长度、宽度和厚度,其余部分用硅胶对试样进行密封,待硅胶风干后将试样封于特制溶液盒中待用。
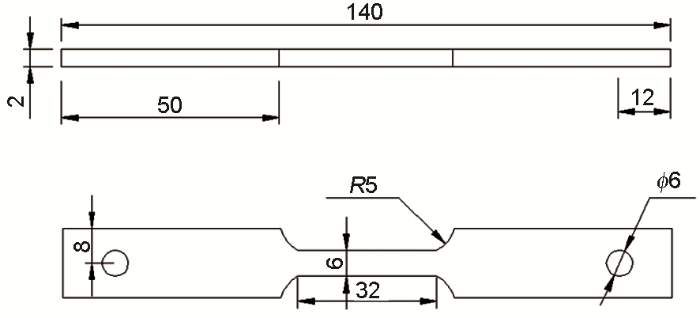
图2 SSRT试样示意图
1.2 SRB培养及实验溶液
实验溶液采用3.5%NaCl模拟海水溶液,用NaCl分析纯加去离子水配制。将其放置在压力蒸汽灭菌器里进行灭菌 (压力蒸汽灭菌器温度为121 ℃),并经紫外灭菌15 min,作为无菌介质。
SRB培养基A由0.5 g/L K2HPO4,0.5 g/L Na2SO4,1 g/L NH4Cl,0.1 g/L CaCl2,2 g/L MgSO4·7H2O,1 g/L酵母粉,3 mL乳酸钠组成;培养基B为0.1 g/L抗坏血酸,0.1 g/L保险粉,0.1 g/L硫酸亚铁铵。用4% (质量分数) NaOH溶液调节培养基A至pH7.2。在121 ℃压力蒸汽灭菌器里消毒15 min,培养基B经圆筒式过滤器紫外线杀菌处理。实验前将实验溶液及实验器材用压力蒸汽灭菌器在121 ℃下高温灭菌15 min。溶液在灭菌前持续通入N2气60 min,以保证消除O2。菌种按1∶50比例接种到实验溶液和培养基的混合溶液中,接菌后放入生化培养箱恒温培养至不同时期待用,培养温度为 (30±2) ℃。采用最大可能数 (MPN) 法[26]测定实验溶液中SRB的数量,绘制SRB生长曲线。
1.3 电化学实验
电化学实验在PARSTAT2273型电化学工作站上完成。采用三电极体系,工作电极为2205DSS,辅助电极为Pt电极,参比电极为饱和甘汞电极 (SCE)。在接菌的3.5%NaCl溶液中,对2205DSS在SRB新陈代谢不同时间时进行动电位极化曲线测量。动电位极化曲线的扫描区间为-1.0 V至电流密度为10-2 A/cm2,扫描速率为1 mV/s。为了与无菌条件进行对比,对2205DSS在无菌溶液中浸泡4 d后的电化学行为进行了测量。
1.4 SSRT实验
在WDML-3型应力腐蚀试验机上完成SSRT实验,以10-6 mm/s的拉伸速率对其进行拉伸,记录负荷、位移、时间等相关参数。实验后对主断口及其侧断口形貌用SU8010型扫描电子显微镜 (SEM) 进行观察。拉伸试样取平行样3个,最终结果取3个平行样测试结果的平均值。
为了进一步探究SRB对2205 DSS在3.5%NaCl溶液中腐蚀敏感性的影响,测量SSRT实验试样断裂前后尺寸的变化,通过伸长率δ、断面收缩率ε来评定SCC敏感性,计算如下:
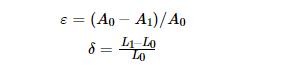
其中,A0和A1分别为初始横截面和试件拉断后颈缩处截面积;L0和L1分别为原标距长度和拉伸断裂后长度。
2 实验结果
2.1 SRB生长曲线
图3为SRB在3.5%NaCl溶液中的生长曲线。可以看出,SRB的生长过程可分为3个阶段。1~3 d为对数生长期,这段期间营养充足使SRB迅速繁殖,数量呈对数生长且活性增强。4~8 d是稳定生长期,在这个阶段SRB数量有小范围的浮动,但繁殖和死亡速率基本相等。9~14 d进入SRB的衰亡期,此时由于有菌介质中培养基的营养物质供给不足导致SRB数量急剧下降。
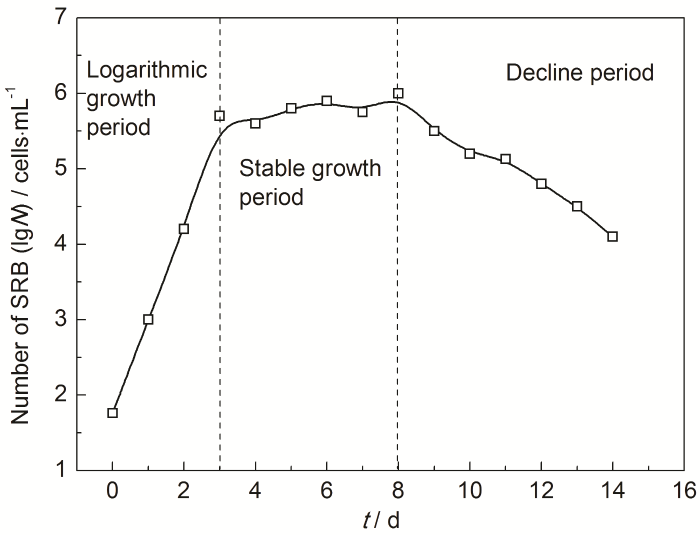
图3 SRB在3.5%NaCl溶液中的生长曲线
2.2 极化曲线
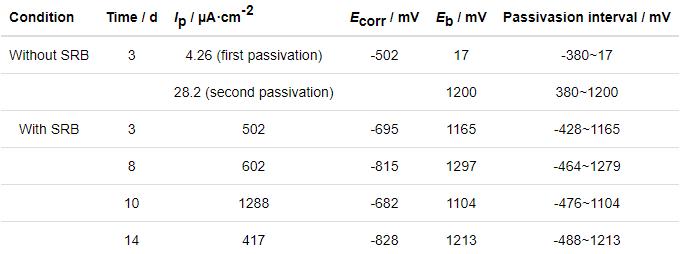
根据SRB生长曲线,分别在第3,8,10和14 d对2205DSS在有菌的3.5%NaCl溶液中进行了动电位极化曲线测量,结果见图4,极化曲线拟合得到的相关参数见表1。根据表1和图4中的结果可以看出,Ecorr在有菌时明显降低,表明SRB的活性增加了2205DSS发生腐蚀的热力学倾向。由图4可知,与无菌溶液中相比,SRB的存在显著改变了阳极极化曲线形状。在无菌溶液中,阳极极化曲线显示出两段钝化行为:在电位区间-380~17 mV时,2205DSS表现为一次钝化,钝化电流Ip1为4.26 μA/cm2;在电位区间380~1200 mV时,表现为二次钝化,钝化电流Ip2为28.2 μA/cm2。文献[1]表明,2205DSS钝化膜一般为双层结构,外层富含Fe的氧化物,而内层富含Cr的氧化物。2205DSS在无菌3.5%NaCl溶液中的两次钝化行为表明,在电位较低时,钝化膜中Fe的氧化物起保护作用,随阳极极化程度增加,Fe的氧化物被逐渐溶解,露出内层Cr的氧化物,极化曲线进入二次钝化区。当Cr的氧化物被阳极溶解后,钝化膜消失,露出钢基体,极化曲线也随之进入过钝化区。而当溶液中含有SRB时,所有极化曲线均显著右移,一次钝化均消失,表明第3 d时,2205DSS钝化膜外层Fe的氧化物已经被SRB腐蚀。此外,有菌介质中的腐蚀电流密度还大于无菌溶液中二次钝化电流,这表明内层Cr的氧化物也已经发生了退化。因此,有菌介质中的钝化行为应该是SRB导致的腐蚀反应产生的生物膜与腐蚀产物膜提供的。由表1拟合结果可知,随着SRB开始进入稳定生长期,电极表面开始形成较为完整的生物膜,腐蚀电流Ip随SRB数量的增加而增大。Ip在第10 d达到最大值,为1288 μA/cm2,几乎为无菌时的45倍。此外,8~14 d的阳极极化曲线在0 V处出现明显的阳极峰,这可能是由于形成的生物膜与腐蚀产物膜造成的,表明SRB的存在改变了2205DSS的阳极反应。随着SRB的死亡,Ip明显降低,甚至低于第3 d,但仍为无菌时的14倍,说明SRB代谢产物显著加速了2205DSS的腐蚀过程。
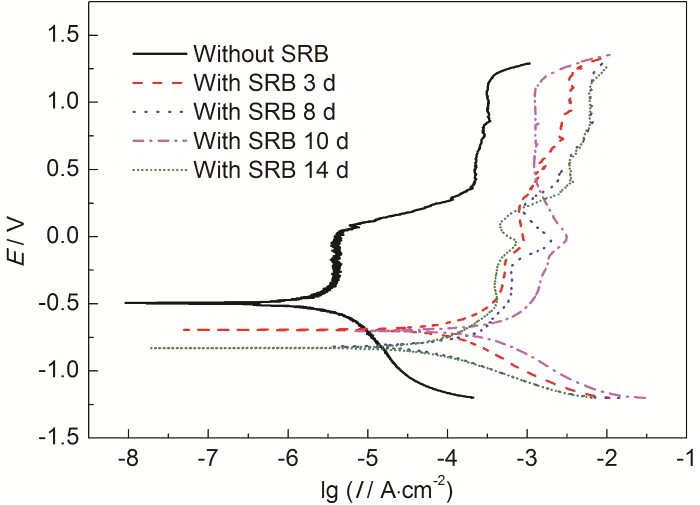
图4 2205DSS在3.5%NaCl溶液中的极化曲线
表1 2205不锈钢在3.5%NaCl溶液中动电位极化曲线拟合结果
2.3 SSRT结果
2205DSS在无菌和含SRB的3.5%NaCl溶液中不同生长阶段的应力-应变曲线如图5所示。可以看出,在无菌时应变所需断裂能较大,几乎与空拉相同,抗拉强度最大,达到751.0 MPa。在有菌时,各条件下的应变值均小于在无菌介质中的应变,表明SRB的存在增加了2205DSS的SCC敏感性。SSRT曲线在SRB生长至第8 d时应变最小,表明此时SCC敏感性最大。此时抗拉强度达到最小,仅为623.9 MPa。而在第3,10和14 d时应变相差不多,SCC敏感性较小。
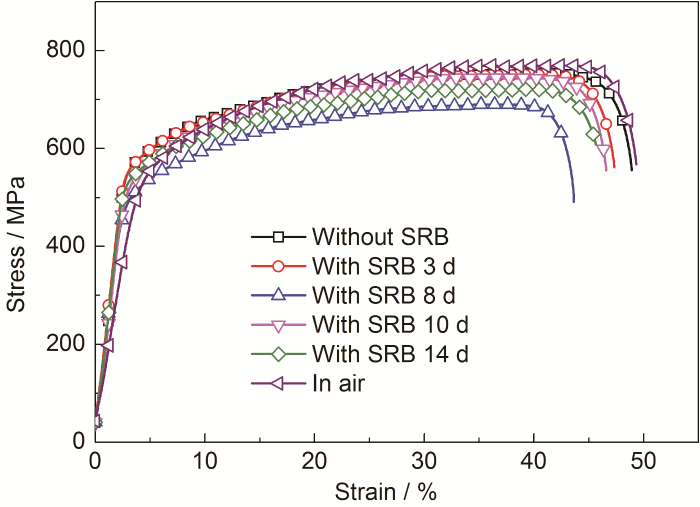
图5 2205DSS在3.5%NaCl溶液中浸泡不同时间的慢拉伸应力-应变曲线
2205DSS在3.5%NaCl溶液中浸泡不同时间的伸长率δ和断面收缩率ε的结果如图6所示,其中用0 d表示无菌溶液。可以看出,δ和ε在第8 d时最小。伸长率和断面收缩率结果与SRB生长曲线规律呈对应关系,即伸长率和断面收缩率在SRB生长较为旺盛的稳定期达到最小,此时2205DSS的脆性增强,抗变形能力最差,SCC敏感性最强。值得注意的是,随着SRB进入衰亡期,断面收缩率并未随应变减小而降低,这表明此时脆性断裂敏感性低于第8 d时的。
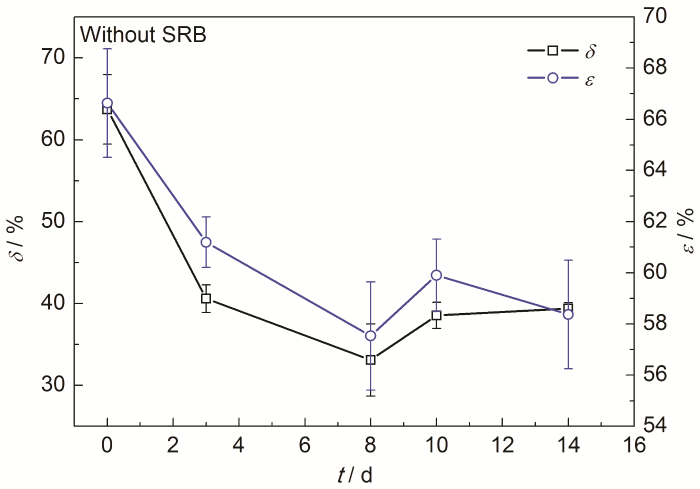
图6 SSRT后2205DSS伸长率和断面收缩率的变化曲线
2.4 断口形貌观察
为了更进一步研究SRB新陈代谢对2205DSS在3.5%NaCl溶液中SCC机制的影响,对拉伸试样主断口和侧断口形貌进行了SEM观察,结果见图7。在无菌溶液中,2205DSS断口呈现出典型的穿晶韧性断裂模式 (图7a1),局部韧窝壁上有蛇形滑移特征。在大且深的韧窝周围可以观察到由小孔或者小孔构成的格状表面,这种大且深和小微孔的结构表明了微观奥氏体和铁素体双相结构在2205钢开裂过程中的作用[27]。侧断口表面光滑,没有任何点蚀坑和裂纹 (图7a2)。在含SRB的3.5%NaCl溶液中,浸泡3 d时2205DSS主断口还是以韧窝为主 (图7 b1),韧窝大小与深度较无菌时明显减小,但仍呈现韧性断裂特征,局部伴随较深微孔。侧断口随着拉伸方向出现规则的位错滑移现象 (图7b2),但并未出现裂纹。当SRB生长至第8 d时,断口较平整 (图7c1),韧窝数量显著减少,呈现出以脆性断裂为主的混合型断裂。断口内呈现明显的α铁素体穿晶解理为主、γ奥氏体韧性撕裂的准解理型特征,这是典型的双相不锈钢氢致应力开裂断口形貌[28,29]。由于α和γ相对氢脆敏感性不一致,α相对氢脆敏感性相对较高[30,31]。因此当SRB代谢产生的H进入钢中,γ相能保持一定的韧性,但α相则表现出较高的脆性。在铁素体的断裂面上观察到特征性的河流型。当解理断裂被迫在晶界处以不同的方向重新启动,并趋向于沿着裂纹扩展方向合并时,就形成了这些“河流型”形貌[30]。侧断口出现了深且宽的二次裂纹 (图7c2),裂纹萌生于较大的点蚀坑,且宽浅坑底部出现次生点蚀。之后在第10 和14 d,尽管断口具有韧性和准松弛性 (图7d1和7e1),但侧断口有二次裂纹的严重程度有所增加 (图7d2和7e2),表明仍存在SCC敏感性。

图7 2205DSS在不同条件下主断口和侧断口形貌
3 分析与讨论
与无菌溶液中相比,2205DSS试样在有菌3.5%NaCl溶液中极化曲线的Icorr大5倍以上,Ecorr比在无菌溶液中更负,即发生腐蚀的热力学倾向更大 (图7c1)。2205DSS在无菌3.5%NaCl溶液中,发生以下电化学反应:
阳极反应:

阴极反应:

在无菌溶液中2205DSS延伸率和断口收缩率较大,且断口呈现典型的韧性断裂,表明此时2205DSS不具有SCC敏感性。而在厌氧有菌介质中,体系中发生以下电化学反应[21,22,32]:
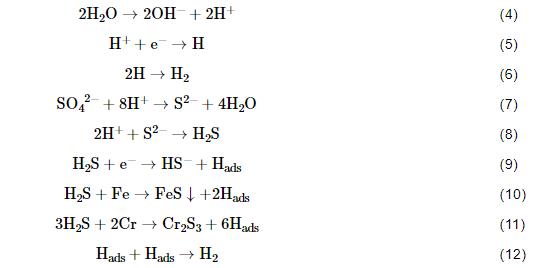
当SRB处于对数生长期时,菌落迅速吸附在2205DSS电极表面,产生胞外聚合物 (EPS) 等[22,33]。在第3 d,对数增长期结束后,随着SRB数量的增加,电极表面形成了较为完整的具有保护作用的生物膜,阻碍了金属与介质的接触。此时溶液中SRB数量虽较多,但由于SRB繁殖时间较短,且生物膜较为完整,溶液中代谢产物较少,对2205DSS的SCC行为影响较小。因此在第3 d时,2205DSS在有菌溶液中表现为韧性断裂,且试样表面没有明显的腐蚀,断面收缩率和延伸率较大,此时SCC敏感性较小。当SRB生长至第8 d时,SRB的新陈代谢最旺盛,代谢产物中产生浓度较大的包含能够促进H渗透的产物,如H2S,HS-和S2-等,其中H2S具有毒化作用[34],它能催化促进生成H,又同时阻碍H结合成H2的进行,从而在钢表面保持较高的H浓度。一部分H结合形成H2从溶液中逸出;然而另一部分H吸附在金属表面,进入金属晶格,在微观结构缺陷位点分离,扩散到裂纹尖端区域并富集,诱发裂纹萌生,加速金属的裂纹扩展[21]。SRB对腐蚀的加速作用表现为,一是SRB为了维持自身生理代谢活动通过还原SO42-和氧化有机分子获得必要的能量而产生S2-,同时借助产生的S2-与H+在溶液中结合形成H2S[22];二是生成的H2S加强了H在钢表面的吸附并降低H的复合速率[32]。然后,吸附的氢 (Hads) 进入钢材,扩散到应力高的塑性区,产生裂纹,导致钢材脆化[35]。此时SRB有类似氢化物的作用[36]。因此在SRB活性浓度最大的第8 d时,应变最小,断面收缩率损失系数和延伸率损失系数最大,呈现以脆性为主脆性混合断裂特征。此外,第8 d时,侧断口出现了明显的点蚀坑 (图7c2)。Dec等[37]研究证明,与无S钝化膜相比,含S钝化膜更容易被Cl-穿透而加速腐蚀,因此SRB新陈代谢产生的硫化物为Cl-穿透提供了“通道”,进而为SCC提供了诱发点。点蚀坑底部出现次生点蚀坑,表明SRB诱发了二次点蚀,二次点蚀可使宽浅坑的应力集中程度增大,从而导致“二次开裂”,Wu等[23]认为二次点蚀的出现是SRB与弹性应力的协同作用导致的。由此可见,在第8 d时2205DSS发生SCC的机理为阳极溶解和氢脆共同控制的混合断裂机制。
此外,SEM分析结果表明,2205DSS中的奥氏体相和铁素体相在SCC过程中表现出不同的敏感性。铁素体相具有较高的强度,但比奥氏体相更脆;与高含氮的奥氏体相比,铁素体相是阳极的[25]。因此,铁素体与氢的相互作用导致了力学性能或相变等方面的变化不同于奥氏体,表现出更高的SCC敏感性。
随着SRB进入衰亡期 (第10和14 d),SRB新陈代谢能力逐渐减弱,细胞相继死亡,活性SRB浓度变小。尽管与第8 d相比,此时断面收缩率和延伸率略有增加,断口变为韧性-脆性混合断裂特征,但侧断面二次裂纹表明,与无菌条件下相比,其SCC敏感性仍较高。这主要是由于SRB代谢产物 (H2S,HS-和S2-等) 在溶液中仍有一定浓度造成的。由此可见,SRB活性浓度与2205DSS的SCC敏感性呈正相关,SRB的生理代谢活动会促进SCC的发生,SRB活性越大,其SCC敏感性越高。
4 结论
(1) SRB的存在改变了2205DSS在3.5%NaCl溶液中阳极极化反应的进程,增强了2205DSS腐蚀的热力学倾向,诱发点蚀,为SCC提供了裂纹形核点。
(2) 2205DSS在无菌3.5%NaCl溶液中不具有SCC敏感性。SRB存在时,其SCC敏感性显著增加。
(3) 2205DSS的SCC敏感性与SRB活性浓度呈正相关,SRB活性浓度越大,SRB对SCC促进作用越强。在SRB处于稳定生长期,其代谢产物增加了钢的脆性,其SCC机理为阳极溶解和氢脆混合控制机制。而SRB在其他生长阶段,2205DSS的SCC敏感性虽较小,但仍高于在无菌介质中的。
(4) SRB作用下,2205DSS中铁素体相表现为穿晶解理特征,奥氏体相表现为韧性撕裂的特征,铁素体相具有更高的SCC敏感性。
参考文献
1 Yassar R S, Scudiero L, Alamr A S, et al. Microstructure-mechanical and chemical behavior relationships in passive thin films [J]. Thin Solid Films, 2010, 518: 2757
2 Vignesh K, Perumal A E, Velmurugan P. Resistance spot welding of AISI-316L SS and 2205 DSS for predicting parametric influences on weld strength-Experimental and FEM approach [J]. Arch. Civ. Mech. Eng., 2019, 19: 1029
3 Sozańska M, Kyk-Spyra K. Investigation of hydrogen induced cracking in 2205 duplex stainless steel in wet H2S environments after isothermal treatment at 675, 750 and 900 ℃ [J]. Mater. Charact., 2006, 56: 399
4 Naghizadeh M, Moayed M H. Investigation of the effect of solution annealing temperature on critical pitting temperature of 2205 duplex stainless steel by measuring pit solution chemistry [J]. Corros. Sci., 2015, 94: 179
5 Sieurin H, Sandstrm R. Austenite reformation in the heat-affected zone of duplex stainless steel 2205 [J]. Mater. Sci. Eng., 2006, A418: 250
6 Lin H X, Fan Y G, Xiong H, et al. Comparision of stress corrosion resistance of 22Cr duplex stainless steel, 304L and 316L common austenitic stainless steels in chloride solutions [J]. Corros. Prot., 2009, 30: 386
6 林红先, 樊玉光, 熊惠等. 22Cr双相不锈钢与304L、316L钢在氯化物溶液中耐应力腐蚀性能的比较 [J]. 腐蚀与防护, 2009, 30: 386
7 Tsai W T, Chen M S. Stress corrosion cracking behavior of 2205 duplex stainless steel in concentrated NaCl solution [J]. Corros. Sci., 2000, 42: 545
8 Wu W, Liu Z Y, Hu S S, et al. Effect of pH and hydrogen on the stress corrosion cracking behavior of duplex stainless steel in marine atmosphere environment [J]. Ocean. Eng., 2017, 146: 311
9 Song Z L, Yang L J, Moradi M, et al. Study on failure behavior of duplex stainless steel in Marine environment [A]. Marine Materials Corrosion and Protection Conference [C]. Beijing: 2014
9 宋振纶, 杨丽景, Moradi M等. 双相不锈钢在海洋环境中的失效行为研究 [A]. 2014海洋材料腐蚀与防护大会论文集 [C]. 北京: 2014
10 Yan T, Song Z L, Yang L J, et al. Effect of Vibrio neocaledonicus sp. on corrosion behavior of copper in artificial sea Water [J]. J. Chin. Soc. Corros. Prot., 2016, 36: 157
10 闫涛, 宋振纶, 杨丽景等. 新喀里多尼亚弧菌对Cu在人工海水中腐蚀行为的影响 [J]. 中国腐蚀与防护报, 2016, 36: 157
11 Wu T Q, Yang P, Zhang M D, et al. Microbiologically induced corrosion of X80 pipeline steel in an acid soil solution: (II) corrosion morphology and corrosion product analysis [J]. J. Chin. Soc. Corros. Prot., 2014, 34: 353
11 吴堂清, 杨圃, 张明德等. 酸性土壤浸出液中X80钢微生物腐蚀研究: (Ⅱ) 腐蚀形貌和产物分析 [J]. 中国腐蚀与防护学报, 2014, 34: 353
12 Liu B, Duan J Z, Hou B R. Microbiologically influenced corrosion of 316l ss by marine biofilms in seawater [J]. J. Chin. Soc. Corros. Prot., 2012, 32: 48
12 刘彬, 段继周, 侯保荣. 天然海水中微生物膜对316L不锈钢腐蚀行为研究 [J]. 中国腐蚀与防护学报, 2012, 32: 48
13 Xu C M, Zhang Y H, Cheng G X, et al. Localized corrosion behavior of 316L stainless steel in the presence of sulfate-reducing and iron-oxidizing bacteria [J]. Mater. Sci. Eng., 2007, A443: 235
14 Rao T S, Nair K V K. Microbiologically influenced stress corrosion cracking failure of admiralty brass condenser tubes in a nuclear power plant cooled by freshwater [J]. Corros. Sci., 1998, 40: 1821
15 Abedi S S, Abdolmaleki A, Adibi N. Failure analysis of SCC and SRB induced cracking of a transmission oil products pipeline [J]. Eng. Fail. Anal., 2007, 14: 250
16 Kholodenko V P, Jigletsova S K, Chugunov V A, et al. Chemicomicrobiological diagnostics of stress corrosion cracking of trunk pipelines [J]. Appl. Biochem. Microbiol., 2000, 36: 594
17 Stipaniev M, Rosas O, Basseguy R, et al. Electrochemical and fractographic analysis of microbiologically assisted stress corrosion cracking of carbon steel [J]. Corros. Sci., 2014, 80: 60
18 Javaherdashti R, Raman R K S, Panter C, et al. Microbiologically assisted stress corrosion cracking of carbon steel in mixed and pure cultures of sulfate reducing bacteria [J]. Int. Biodeterior. Biodegrad., 2006, 58: 27
19 Domalicki P, Lunarska E, Birn J. Effect of cathodic polarization and sulfate reducing bacteria on mechanical properties of different steels in synthetic sea water [J]. Mater. Corros., 2007, 58: 413
20 Raman R K S, Javaherdashti R, Panter C, et al. Hydrogen embrittlement of a low carbon steel during slow strain testing in chloride solutions containing sulphate reducing bacteria [J]. Mater. Sci. Technol., 2005, 21: 1094
21 Wu T Q, Yan M C, Zeng D C, et al. Hydrogen permeation of X80 steel with superficial stress in the presence of sulfate-reducing bacteria [J]. Corros. Sci., 2015, 91: 86
22 Wu T Q, Yan M C, Yu L B, et al. Stress corrosion of pipeline steel under disbonded coating in a SRB-containing environment [J]. Corros. Sci., 2019, 157: 518
23 Wu T Q, Xu J, Yan M C, et al. Synergistic effect of sulfate-reducing bacteria and elastic stress on corrosion of X80 steel in soil solution [J]. Corros. Sci., 2014, 83: 38
24 Huang Y L. Corrosion failure of marine steel in sea-mud containing sulfate reducing bacteria [J]. Mater. Corros., 2004, 55: 124
25 Wang J, Li Q F, Fu Y D, et al. MIC behavior of the low alloy steel with different zn-epoxy coating in SRB solution [J]. Key Eng. Mater., 2011, 488/489: 262
26 Mcgenity T J, Timmis K N, Nogales B. Hydrocarbon and Lipid Microbiology Protocols [M]. Berlin: Springer Protocols Handbooks, 2016
27 abanowski J, Rzychoń T, Simka W, et al. Sulfate-reducing bacteria-assisted hydrogen-induced stress cracking of 2205 duplex stainless steels [J]. Mater. Corros., 2019, 70: 1667
28 Chou S L, Tsai W T. Hydrogen embrittlement of duplex stainless steel in concentrated sodium chloride solution [J]. Mater. Chem. Phys., 1999, 60: 137
29 Craidy P, Briottet L, Santos D. Hydrogen-microstructure-mechanical properties interactions in super duplex stainless steel components [J]. Int. J. Hydrog. Energ., 2015, 40: 17084
30 Silverstein R, Eliezer D. Hydrogen trapping mechanism of different duplex stainless steels alloys [J]. J. Alloy. Compd., 2015, 644: 280
31 Huang Y L, Cao C N, Lin H C, et al. Effects of hydrogen on the scc of austeniticstainless steel in acidic chloride solution [J]. Studia Marina Sin., 1998, (40): 109
31 黄彦良, 曹楚南, 林海潮等. 氢对奥氏体不锈钢在酸性氯离子溶液中SCC作用初探 [J]. 海洋科学集刊, 1998, (40): 109
32 Sowards J W, Williamson C H D, Weeks T S, et al. The effect of Acetobacter sp. and a sulfate-reducing bacterial consortium from ethanol fuel environments on fatigue crack propagation in pipeline and storage tank steels [J]. Corros. Sci., 2014, 79: 128
33 Liu J H, Liang X, Li S M. Study of microbiologically induced corrosion action on Al-6Mg-Zr and Al-6Mg-Zr-Sc [J]. J. Rare Earth., 2007, 25: 609
34 Yang Z, Huo C Y, Zhu Y Y, et al. Stress corrosion cracking of X70 grade line pipe steel in H2S aqueous solutions [J]. Mar. Sci., 2005, 29(10): 23
34 杨洲, 霍春勇, 朱永艳等. 硫化氢对管线钢在氯化钠溶液中应力腐蚀开裂的影响 [J]. 海洋科学, 2005, 29(10): 23
35 Zucchi F, Grassi V, Monticelli C, et al. Hydrogen embrittlement of duplex stainless steel under cathodic protection in acidic artificial sea water in the presence of sulphide ions [J]. Corros. Sci., 2006, 48: 522
36 Wu T Q, Sun C, Yan M C, et al. Sulfate-reducing bacteria-assisted cracking [J]. Corros. Rev., 2019, 37: 231
37 Dec W, Mosiaek M, Socha R P, et al. Characterization of Desulfovibrio desulfuricans biofilm on high-alloyed stainless steel: XPS and electrochemical studies [J]. Mater. Chem. Phys., 2017, 195: 28
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





