摘要
选取了9C系列铝合金9C34 (挤压成形) 和9C37 (模压成形) 以及美国5083铝合金进行对比研究,通过拉伸实验及硬度测试对比评估了各铝合金力学性能,通过盐雾实验、极化曲线和阻抗谱测试考察温度和pH对3种铝合金在不同腐蚀环境中腐蚀行为的影响规律。结果表明:9C铝合金的强度可达550 MPa,硬度为130HB,都显著高于5083铝合金的。在实验的不同温度与pH腐蚀环境中,9C铝合金同时具有与美国5083铝合金相当的优异耐蚀性,作为耐腐蚀结构材料具有明显的应用优势。
关键词: 铝合金 ; 粉末冶金 ; 耐蚀性 ; 腐蚀行为 ; 力学性能
Al及其合金因密度小、比强度高、导电导热性能高、易加工成型等优点,在建筑、航空、机械、交通、化工、仪器仪表、电子电器、食品轻工以及人民日常生活的各个领域里都得到广泛的应用[1]。但是,目前传统铝合金锻造工艺材料损耗严重,成本较高,且难以制造一些形状比较复杂的产品[2];而铸造成形虽可以生产出形状复杂的零件且成本较低,但在凝固过程中易形成成分偏析、缩松、缩孔等缺陷,这些缺陷极大的影响到材料的耐蚀性及力学性能,很难达到材料的最佳性质[3]。
9系铝合金是一类通过粉末冶金技术制备的高性能铝合金材料,其显微组织结构得到显著细化,组分也有别于传统铝合金。该系列材料是中国科学院长春应用化学研究所开发并进行产业化孵化[4],但其耐蚀性能尚未进行系统研究。
本文选取了9C系列粉末冶金铝合金中的两个牌号9C34 (挤压成形)、9C37 (模压成形) 与美国5083铝合金进行对比研究。通过拉伸实验及硬度测试评估各铝合金力学性能,通过盐雾实验、极化曲线和阻抗谱测试考察温度和pH对各铝合金在不同腐蚀环境中腐蚀行为的影响规律,为粉末冶金高强高耐蚀铝合金在海洋领域的应用提供参考。
1 实验方法
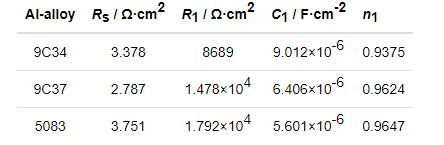
9C34和9C37铝合金的化学成分 (质量分数,%) 为:Al 98.0、Mg 1.5、Mn 0.3、Si 0.2。5083铝合金化学成分 (质量分数,%) 为:Mg 4.0~4.9、Mn 0.4~1.0、Cr 0.1~0.3、Fe 0.4、Zn 0.2、Cu 0.1,Al余量。
根据GB/T228.1-2010在万能试验机上进行拉伸试验。试件尺寸为8 mm×3 mm,依次使用乙醇、去离子水在超声波清洗器中对样品进行彻底清洗以去除表面油污,每组试样测试3个样并求平均值。根据GB/T231.1-2018在TH600数显布氏硬度计上测试硬度,选用直径为10 mm的压头,实验力为1500N,每个表面测试5次硬度值求平均值。根据GB/T10125-2012在FLSP-100A盐雾试验箱中进行盐雾腐蚀试验。中性盐雾实验参数如下:NaCl溶液浓度为50 g/L,pH为6~7,温度为 (35±2) ℃,喷雾量 (平均沉降率) 为1~2 mL/80 (cm2·h)。分别于盐雾实验72、144、216和288 h后取样 (每次平行样4片),将试样置于68%浓硝酸中超声清洗2 min,经自来水漂洗后再以去离子水、乙醇超声清洗,80 ℃烘干2 h,冷却到室温后精确称重。
在CHI660E电化学工作站上采用三电极体系进行电化学测试。将封装制备的铝合金电极作为工作电极,参比电极为饱和甘汞电极 (SCE),惰性电极为20 mm×20 mm的铂片。电化学阻抗谱的测量在开路电位下进行,频率范围为105~10-2 Hz,正弦波幅值为10 mV。极化曲线扫描的范围为相对于开路电位±0.5 V,扫描速率为1 mV·s-1。
测试溶液为根据GB/T19746-2018在实验室条件下配置的模拟海水,其组成 (g·L-1) 为:NaCl 24.539,MgCl2 5.227,Na2SO4 4.093,CaCl2 1.162,KCl 0.695,NaHCO3 0.201,KBr 0.101,H3BO3 0.027,SrCl2 0.025,NaF 0.003。模拟海水温度控制在25 ℃,用HNO3或NaOH溶液 (50 g/L) 将模拟海水溶液pH分别调至5.0、7.0、8.3;考察温度的影响时,模拟海水pH控制在8.3,通过加冰块或水浴加热的方式将溶液温度分别调至15、25和35 ℃。
2 结果与讨论
2.1 力学性能
图1所示为3种合金的应力-应变曲线。9C34及9C37铝合金拉伸曲线形状与5083铝合金存在较大的差异,随着应变的增加,二者并未出现均匀塑性变形,伸长率分别为4.80%、4.54%,屈强比接近于1,呈现较大的脆性。5083铝合金在形成缩颈后,应力急剧下降,发生断裂时伸长率达到6.69%,表现为较好的塑性。
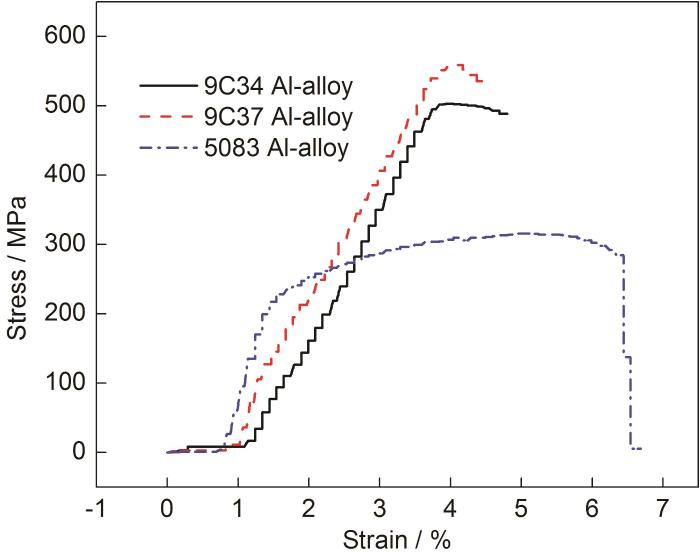
图1 3种铝合金的应力-应变曲线
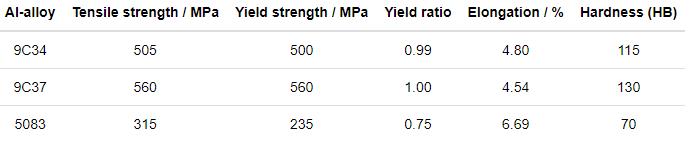
由表1材料力学性能参数可见,与5083铝合金相比,9C34与9C37铝合金具有更高的抗拉强度、屈服强度与硬度。这是因为粉末冶金方法避免了传统变形铝合金易出现的缩松、缩孔、枝晶偏析等缺陷,获得的是无枝晶的均匀细晶组织[5],提高了材料的力学性能。
表1 3种铝合金的力学性能参数
2.2 盐雾腐蚀
图2为3种铝合金不同时间盐雾腐蚀后的宏观形貌。腐蚀初期,表面颜色变暗,出现较多的点蚀坑。随着时间的延长,部分点蚀坑逐渐向深度方向发展为蚀孔,也存在一些点蚀坑向周围扩展成为腐蚀斑。到腐蚀后期,表面腐蚀形貌发展为广度和深度方向都明显可见的溃疡腐蚀,出现较多的局部腐蚀。

图2 3种铝合金不同时间盐雾腐蚀实验后的宏观形貌
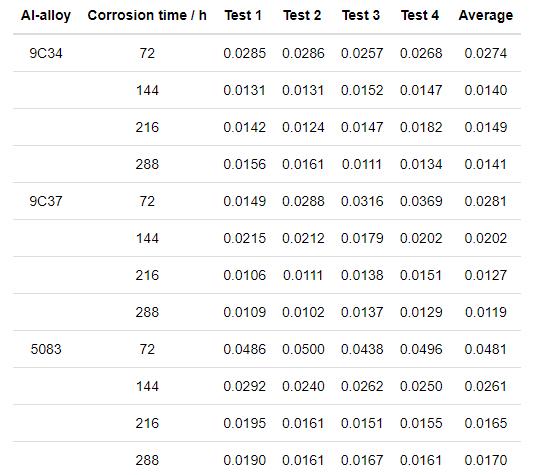
表2所示为9C34、9C37和5083铝合金在盐雾腐蚀不同时间范围内的平均腐蚀速率。从表中可以看出,各铝合金腐蚀速率呈现大致相同的变化趋势,即随着腐蚀时间的延长,平均腐蚀速率不断降低并逐渐趋于平稳。腐蚀初期,3种铝合金均具有较高的腐蚀速率,此时铝表面氧化膜比较薄且不够致密,Cl-易于穿透,铝基体不断受Cl-侵蚀并局部活化溶解;随着时间的延长,铝合金表面的氧化膜逐渐增厚且变得致密和连续,Cl-不易于穿透,腐蚀速率逐渐减慢[6]。此外,实验过程中腐蚀产物在表面不断堆积,阻止或减缓Cl-对基体的腐蚀。整体来看,在35 ℃中性腐蚀介质条件下,9C34和9C37铝合金腐蚀速率始终低于5083铝合金,粉末冶金铝合金的耐蚀性能优于5083铝合金。
表2 3种铝合金在盐雾腐蚀不同时间范围内的平均腐蚀速率
2.3 电化学腐蚀
图3为3种铝合金在模拟海水溶液中的极化曲线,表3为在模拟海水溶液中极化曲线所对应的电化学参数。可以看出,各铝合金试样极化曲线变化趋势大致相同,表明粉末冶金铝合金与5083铝合金腐蚀过程基本相同。各极化曲线中,阴极Tafel斜率均明显小于阳极Tafel斜率;并且在阳极极化区随着过电位的增加,电流密度并没有明显的提升,呈现一段平缓的钝化区,这是因为此时在各铝合金表面生成一层钝化膜[7],使其具有较好的抵抗离子侵蚀的能力。发生的主要反应为Al(ss)-3e-+3OH-=Al(OH)3,ads,其中,ss表示裸露的铝表面,ads表示反应过程中伴随着物种的吸附。中间产物吸附在界面,进一步反应成为最终产物。当过电位增加到一定程度时,钝化膜被击穿,9C34、9C37、5083铝合金的击穿电位分别-0.52、-0.61和-0.64 V,维钝电流分别为6.61×10-6,1.76×10-5和8.54×10-7 A/cm2。5083铝合金击穿电位负于9C34、9C37铝合金的,但其维钝电流比9C34铝合金小1个数量级,比9C37铝合金小2个数量级,说明5083铝合金在阳极极化过程中生成的钝化膜更致密均匀。随着过电位的继续增加,暴露的铝基体受到腐蚀,阳极极化行为受活性溶解过程控制[8],电流密度迅速增加。在阴极极化区,初始阶段,腐蚀电流密度增加遵循Tafel定律,阴极极化反应为O2+2H2O+4e-=4OH-。当阴极过电位增加到一定程度时,由于溶液中溶解氧量减少,阴极反应逐步以析氢反应为主:2H2O+2e-=H2↑+2OH-,腐蚀电流密度增速增加。
图3 3种铝合金在25 ℃,pH8.3模拟海水溶液中的极化曲线
表3 极化曲线拟合参数
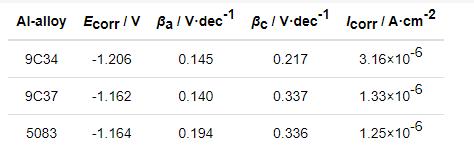
从腐蚀热力学与动力学角度来看,腐蚀电位越正,腐蚀电流密度越小,相应的材料在一定介质中的耐腐蚀性能越好[9]。从表3可以看出,9C34铝合金自腐蚀电位负于其它两种铝合金的,且自腐蚀电流密度较大,这表明在日常海水条件下,9C34铝合金的耐蚀性较9C37铝合金及5083铝合金的差。9C37铝合金腐蚀电位比5083铝合金腐蚀电位正0.002 V,但是腐蚀电流密度比5083铝合金腐蚀电流密度大0.08×10-6 A/cm2,两者抵抗离子侵蚀的能力相差不大,均具有优异的耐腐蚀性。
图4为3种铝合金在模拟海水溶液中的Nyquist图谱及其所对应的等效电路。各铝合金阻抗谱均由高频容抗弧、中频感抗弧及低频容抗弧组成,粉末冶金铝合金与5083铝合金的腐蚀过程相同。低频容抗弧与表面氧化膜的生长与溶解有关,发生的主要反应为Al(ss)+OH-→Al(OH)ads+e-;中频感抗弧是由吸附中间物引起的,发生的主要反应为Al(OH)ads+2OH-→Al(OH)3,ads+2e-;高频容抗弧对应电荷转移电阻与界面双电层电容[10]。
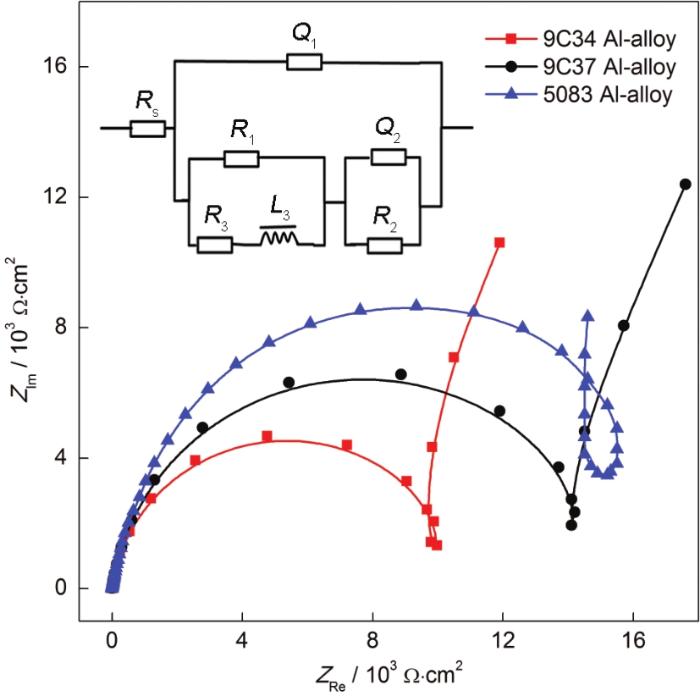
图4 3种铝合金在25 ℃,pH8.3模拟海水溶液中的Nyquist谱及其等效电路[10]
对于电化学阻抗谱的解释,Macdonald等[11]认为阻抗谱中的复杂特征是由腐蚀过程中的具体电化学反应引起的,铝合金在碱性溶液中的电化学溶解过程主要由表面氧化膜的失稳溶解及暴露铝基体的活性溶解组成。
发生在活性点上的基元反应可以用下述反应方程式描述[12]:
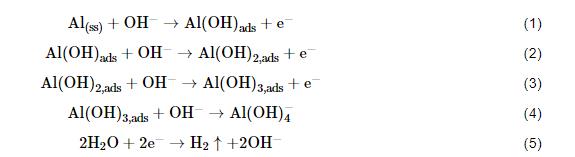
图4b为该条件下阻抗图谱所对应的等效电路。其中,Rs为溶液电阻,Q1和R1分别为界面双电层电容及电荷转移电阻。铝合金表面在腐蚀过程中并非理想电容,存在弥散效应,因而采用常相位角元件Q表示电容,其阻抗可表示为:ZQ=[Y0(jω)n]-1。其中,ω为交流信号的角频率;j=,为虚数单位;Y0为容抗导纳模值;n(0~1) 为弥散系数,其大小取决于电极表面的粗糙程度和腐蚀电流密度分布的不均匀程度,n越接近1表明Q越接近理想电容,n越偏离1表明弥散效应越强[13]。
采用ZsimpWin软件根据该等效电路对阻抗谱进行拟合,通过公式C=Y0(2πfm)n-1将常相位角元件拟合结果换算成相应的等效电容 (fm为常相位角元件对应容抗弧半圆最高点的频率)[14],等效元件的具体参数示于表4中。可以看出,5083及9C37铝合金电荷转移电阻均远远大于9C34铝合金的,在日常海水条件下二者抵抗离子侵蚀的能力更强,耐蚀性更好。C值为Q的等效电容值,其表达式为:
,(S为双电层中金属表面的面积,d双电层电容厚度,εo、εr分别为真空介电常数及膜介电常数)[15]。3种铝合金对应的电容值大小表现为:9C34>9C37>5083,9C34铝合金电容值最大,这是因为腐蚀过程中较多的蚀孔增加了双电层中金属表面的面积,相应的电容值变大[16]。指数n1大小表现为:5083>9C37>9C34,9C34铝合金指数n1更偏离1,表面受腐蚀程度最严重。由于腐蚀产物在表面的堆积或腐蚀坑的产生,表面变粗糙,腐蚀电流密度分布的不均匀程度变大[17]。综上,3种铝合金耐蚀性表现为:5083>9C37>9C34。
表4 3种铝合金在25 ℃碱性模拟海水溶液中等效电路元件拟合结果
2.3.1 不同温度条件下的腐蚀
控制模拟海水pH为8.3,通过在水浴槽中加冰块或加热的方式将溶液温度分别调至15、25和35 ℃,在三电极体系中对各铝合金的电化学腐蚀行为进行具体的分析测试。
图5所示为各铝合金在不同温度模拟海水溶液中的极化曲线。各铝合金试样在不同条件下的极化曲线趋势大致相同,说明在不同温度的腐蚀环境中,粉末冶金铝合金与5083铝合金腐蚀过程基本相同。
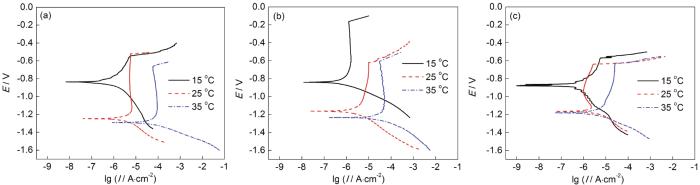
图5 3种铝合金在pH8.3的不同温度模拟海水中的极化曲线
表5为根据极化曲线分析计算出相关电化学参数。受温度变化对铝自由能和侵蚀性离子热运动的影响,随温度升高,各铝合金腐蚀电流密度增大,耐蚀性变差,受腐蚀程度越来越严重。对比同一温度条件下各铝合金的腐蚀电流密度进而对各铝合金耐蚀性进行具体的比较分析:各温度条件下,5083及9C37铝合金腐蚀电流密度均低于9C34的,二者耐蚀性始终优于9C34铝合金。15 ℃下,9C37铝合金腐蚀电流密度大于5083铝合金,其耐蚀性差于5083铝合金;随温度升高,到25 ℃时两者耐蚀性相当;35 ℃下,9C37铝合金腐蚀电流密度小于5083铝合金腐蚀电流密度,其耐蚀性开始强于5083铝合金。9C37铝合金在温度不断变化的环境中具有更加稳定的耐蚀性,并在高温下呈现优异的耐腐蚀性,这与粉末模压试样晶粒细化、组织均匀、致密性好有关[3]。
表5 3种铝合金在pH8.3的不同温度模拟海水中的极化曲线拟合参数
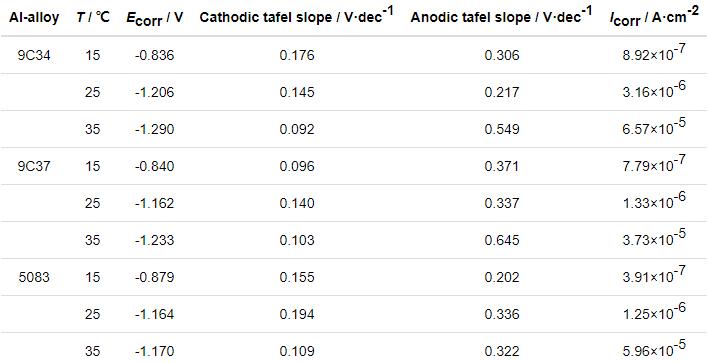
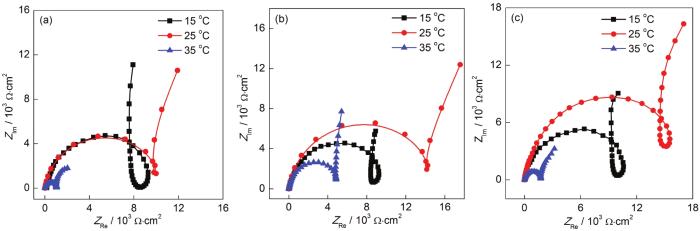
图6所示为各铝合金在pH8.3的不同温度模拟海水溶液中的阻抗图谱。温度条件的变化对各铝合金在模拟海水条件下的腐蚀行为并没有显著的影响。各铝合金在不同温度条件下的阻抗谱均由高频容抗弧、中频感抗弧及低频容抗弧组成。且随温度降低,各铝合金中频感抗弧均表现为越来越大。这是因为中频感抗弧主要由吸附中间物引起,发生的主要反应为Al(OH)ads+2OH-→Al(OH)3,ads+2e-。随温度降低,铝合金在海水中的自由能及OH-热运动均大大降低,整个腐蚀过程减缓,吸附中间产物变多,相应的其对应的感抗弧越来越大。
图6 3种铝合金在pH8.3不同温度模拟海水溶液Nyquist谱
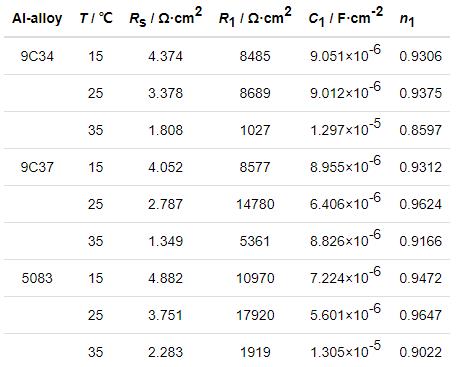
采用ZsimpWin软件根据图4b等效电路对阻抗谱进行拟合,等效元件的具体参数示于表6中。从腐蚀热力学角度看,不同温度条件下,各铝合金的电荷转移电阻均表现为25 ℃>15 ℃>35 ℃,25 ℃环境中耐蚀性最好。这是因为温度对铝合金在碱性环境中铝的自由能和OH-热运动的影响很大,这直接影响到Al(OH)3保护膜的状态和腐蚀行为。如式1~5所示,碱性环境中铝合金表面不断发生着Al(OH)3保护膜的生成和溶解破坏两种化学行为并趋向一个平衡点。与此同时,发生在铝合金表面与保护膜界面的析氢反应也由于微小气泡的析出对Al(OH)3保护膜有相当的破坏作用[18]。15 ℃条件下,受铝合金自由能及溶液中离子活跃度的影响,表面反应以Al(OH)3保护膜的生成为主。随温度升高,Al(OH)3保护膜生成速率提高,对基体覆盖程度增强,耐蚀性增强。当温度增加到一定程度时,Al(OH)3保护膜溶解的电化学行为开始占据主导地位,稳定性开始逐渐降低,再加上析氢反应加剧对阻挡层的破坏作用加强,溶解加速,厚度变薄,基体裸露面积和腐蚀点增加,耐蚀性降低[19]。
表6 3种铝合金在pH8.3的不同温度模拟海水溶液中等效电路元件拟合结果
对比同一温度条件下各铝合金的R1对各铝合金耐蚀性进行分析可见:各温度条件下,5083及9C37铝合金电荷转移电阻均大于9C34铝合金,n1值较9C34更接近于1,受蚀后的表面缺陷更少,二者耐蚀性始终优于9C34铝合金。15和25 ℃条件下,9C37铝合金耐蚀性差于5083;随温度升高,到35 ℃时,9C37铝合金R1大于5083铝合金的,其耐蚀性开始强于5083铝合金,9C37铝合金在不同温度的环境中具有更加稳定的耐蚀性。该结论与极化曲线讨论结果一致。
2.3.2 不同pH条件下的腐蚀
控制模拟海水温度为25 ℃,用HNO3或NaOH溶液 (50 g/L) 将模拟海水溶液pH分别调至5.0、7.0、8.3,在不同pH模拟海水条件下对各铝合金进行动电位极化曲线测试,结果如图7所示。中性及酸性条件下极化曲线变化趋势不同于碱性条件下,表现为完全不同的腐蚀过程。pH7.0与pH5.0条件下,阴极Tafel斜率大于阳极Tafel斜率,并且在阴极极化区存在明显的扩散特征,说明阴极反应过程受扩散过程控制[20]。这是因为在中性及弱酸性条件下,阴极反应以氧的还原为主 (O2+2H2O+4e-→4OH-),随着pH降低,溶液中H+浓度增加,电极的阴极过程既有氧的还原反应又有氢气析出反应发生[21],所以在阴极极化区,pH5.0条件下腐蚀电流密度明显大于pH7.0条件下的电流密度。pH7.0条件下,9C34、9C37铝合金在阳极极化区随过电位增加,电流密度并没有明显的提升,反而呈现一小段类似于pH8.3条件下阳极极化区存在的平缓钝化区,表面生成的钝化膜使其具有了较好的抵抗离子侵蚀的能力。随过电位增加,钝化膜很快被击穿,9C34、9C37铝合金击穿电位分别为-0.47和-0.55 V。5083铝合金在pH7.0条件下的阳极反应并没有钝化层的生成,随着过电位的增加,腐蚀电流密度迅速增加,阳极极化过程受点蚀过程控制。
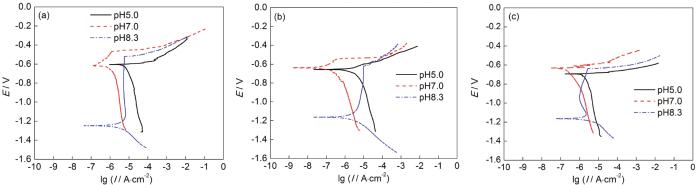
图7 3种铝合金在25 ℃不同pH值的模拟海水溶液中的极化曲线
表7为根据极化曲线分析计算的电化学参数。对比同一pH条件下各铝合金的腐蚀电流密度可以发现,pH5.0条件下,5083铝合金腐蚀电流密度比9C34及9C37铝合金腐蚀电流密度小,各铝合金耐蚀性表现为:5083>9C37>9C34;pH8.3条件下,5083铝合金耐蚀性与9C37铝合金相当,二者耐蚀性均强于9C34铝合金;在pH7.0条件下,9C34及9C37铝合金腐蚀电流密度小于5083铝合金,各铝合金耐蚀性表现为:9C37>9C34>5083。粉末冶金铝合金在中性环境中表现出更好的耐蚀性。
表7 3种铝合金在不同pH的模拟海水溶液中极化曲线拟合电化学参数
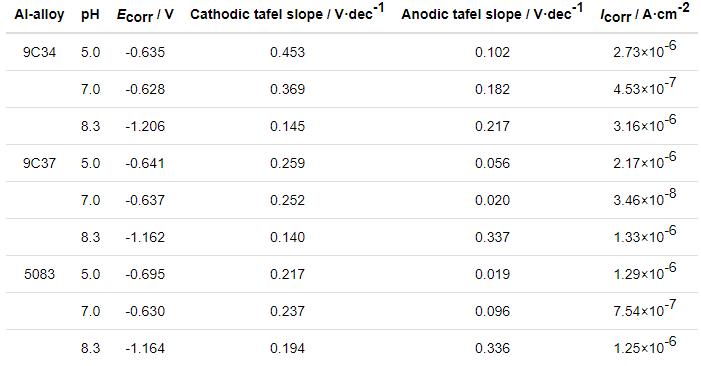
图8为铝合金在不同pH的模拟海水溶液中的Nyquist谱。当pH7.0时,各铝合金Nyquist曲线在低频区均呈现实部电感性收缩现象,表明此时表面尚且处于点蚀的诱导期,侵蚀性阴离子Cl-等吸附在合金表面有缺陷的位置 (位错露头、析出相处等),钝化膜受其侵蚀而尚未穿孔,其主要反应为[22]:
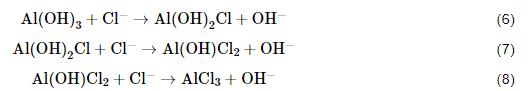
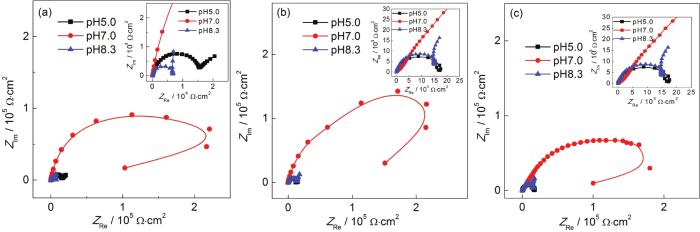
图8 3种铝合金在25 ℃不同pH模拟海水溶液中的Nyquist谱
曹楚南等[23]认为实部电感性收缩随腐蚀程度的增加逐渐减弱,一旦氧化膜穿孔,孔蚀进入发展期,感抗的成分便会消失。如pH5.0时9C37与5083铝合金Nyquist曲线所示,随着pH的降低,氧化膜稳定性降低,受Cl-侵袭越来越严重,低频区实部电感性收缩变小。9C34铝合金pH5.0条件下Nyquist曲线在高频区表现为容抗弧,在低频区表现为一条倾斜45°向上的直线,呈现明显的Warburg阻抗特征,表明电极反应受电荷转移步骤和扩散步骤混合控制。马景灵等[24]认为这是因为随着反应的不断进行腐蚀产物在铝合金表面不断堆积,减缓铝合金表面的溶解,其扩散控制腐蚀过程。陈跃良等[21]认为Warburg阻抗的出现是因为电极表面析氢反应与吸氧反应导致电极表面与溶液存在一定程度的H+浓差与氧浓差,这些物质的扩散引起Warburg阻抗。结合pH5.0条件下9C34铝合金极化曲线,本工作认为陈跃良等的观点更合理。当pH5.0时,9C34铝合金受蚀严重,腐蚀反应剧烈,铝合金表面附近的H+与溶解氧在反应之初便被迅速消耗,本体溶液的H+与溶解氧开始不断地扩散到电极表面发生还原反应,但H+与溶解氧的扩散量始终无法满足电极反应的快速进行,扩散速度不能保证向电极表面供应相应数量的反应物质,电流的大小受限于此扩散速度,该过程表现在Nyquist图中就是一条倾斜45°向上的直线。
图9为不同pH条件下各铝合金阻抗图谱所对应的等效电路。其中,Rs为溶液电阻,Q1和R1分别为界面双电层电容及其电荷转移电阻,Ro与Lo分别表示点蚀活性点的反应电阻及吸附性中间腐蚀产物的弛豫行为,W表示受传质过程控制的Warburg阻抗。
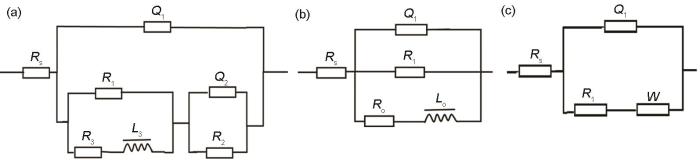
图9 3种铝合金在不同pH模拟海水溶液中阻抗图谱对应的等效电路[25]
采用ZsimpWin软件根据图9所示等效电路对阻抗谱进行拟合,等效元件的具体参数示于表8中。5083、9C37铝合金在pH7.0条件下电感值均远大于pH5.0条件下电感值,该现象表现在阻抗谱中即为pH5.0条件下低频区实部电感性收缩变小,表面腐蚀由点蚀诱导期向点蚀发展期转变。pH7.0条件下,9C34铝合金Nyquist曲线在低频区均呈现实部电感性收缩现象,其电感Lo为7.575×107 H·cm2;当pH5.0时,表面受蚀严重,电极反应受电荷转移步骤和扩散步骤混合控制,其Warburg阻抗的大小为0.392×10-3 Ω-1·cm2。
表8 3种铝合金在25 ℃不同pH值的模拟海水溶液中的等效电路元件拟合结果
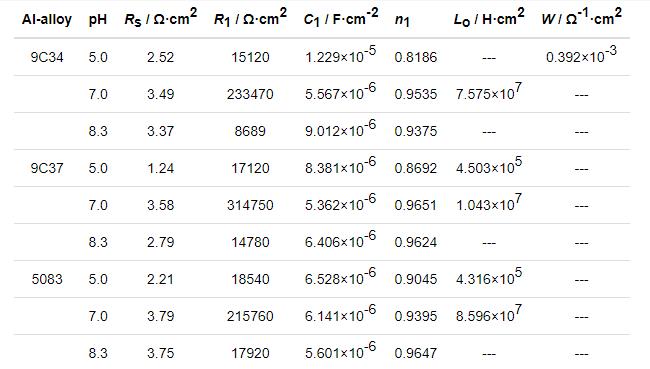
对比同一pH条件下各铝合金的电荷转移电阻进而对各铝合金耐蚀性进行具体的比较分析:pH5.0条件下,5083铝合金电荷转移电阻更大,指数n1更接近1,各铝合金耐蚀性表现为:5083>9C37>9C34。pH7.0条件下,9C34及9C37铝合金电荷转移电阻均大于5083,抵抗离子侵蚀能力更强;9C34及9C37铝合金指数n1较5083更接近于1,受蚀后表面完整度更高。粉末冶金铝合金在pH7.0条件下耐蚀性优于5083,该结论与极化曲线讨论结果一致。
3 结论
(1) 在不同温度与pH的模拟海水溶液中,9C34、9C37铝合金与5083铝合金极化曲线变化趋势和阻抗谱形状一致,粉末冶金铝合金与传统变形铝合金腐蚀过程相同。温度的变化对各铝合金在碱性模拟海水条件下的腐蚀行为并没有显著的影响,各铝合金阻抗谱均由高频容抗弧、中频感抗弧及低频容抗弧组成。溶液pH的增大或减小主要表现在对铝合金表面氧化膜破坏程度的不同,进而表现出不同的耐蚀性。
(2) 粉末冶金铝合金的强度 (可达550 MPa)、硬度 (可达HB130) 等性能指标显著优于5083铝合金的。在35 ℃、中性盐雾腐蚀环境中,粉末冶金铝合金的耐蚀性能优于5083铝合金。在多种不同温度与pH的腐蚀环境中,9C34铝合金耐腐蚀性比美国5083铝合金稍差,而9C37铝合金耐腐蚀性与美国5083铝合金相当。
参考文献
1 Duan L Q. Study on the green sealing methods for aluminum alloy anodic oxide film [D]. Beijing: Beijing University of Chemical Technology, 2010
1 段立清. 铝合金阳极氧化膜的稀土封闭技术的研究 [D]. 北京: 北京化工大学, 2010
2 Li Y D, Liu X H, Zhang X L, et al. An review of semi-solid near-net forming in wrought aluminum alloy [J]. Spec. Cast. Nonferr. Alloys, 2014, 34: 471
2 李元东, 刘兴海, 张心龙等. 变形铝合金半固态近净成形研究进展 [J]. 特种铸造及有色合金, 2014, 34: 471
3 Wang B. The Research on compaction mechanism of 6061 [D]. Wuhan: Wuhan University of Technology, 2018
3 王斌. 6061铝合金粉末压制机理研究 [D]. 武汉: 武汉理工大学, 2018
4 Qu H, Tang H G, Yuan X D, et al. A series of high performance aluminium alloys prepared by powder metallurgy [J]. J. Appliance Sci. Technol., 2016, (): 223
4 曲华, 汤华国, 袁迅道等. 粉末冶金技术制备的系列高性能铝合金 [J]. 家电科技, 2016, (): 223
5 Zhang W L. The influence of powder metallurgy process on the properties of preparation process materials [J]. Adhesion, 2019, 40: 41
5 张万良. 粉末冶金工艺对制备工艺材料性能的影响 [J]. 粘接, 2019, 40: 41
6 Wang J T, Guo Y L, Jin T. Corrosion behavior of Q235A-Z35 steel under 3.5%NaCl salt spray condition [J]. Mater. Prot., 2020, 53(4): 89
6 王建涛, 郭云龙, 金涛. 3.5%NaCl盐雾条件下Q235A-Z35钢的腐蚀行为研究 [J]. 材料保护, 2020, 53(4): 89
7 Cao C N. Principles of Electrochemistry of Corrosion [M]. Beijing: Chemical Industry Press, 2008: 99
7 曹楚南. 腐蚀电化学原理 [M]. 北京: 化学工业出版社, 2008: 99
8 Chen Y L, Wang Z F, Bian G X, et al. Equivalent conversion of galvanic corrosion of typical aluminum-titanium alloy in NaCl solution with different concentrations [J]. Acta Aeronaut. Astronaut. Sin., 2017, 38: 260
8 陈跃良, 王哲夫, 卞贵学等. 不同浓度NaCl溶液下典型铝/钛合金电偶腐蚀当量折算关系 [J]. 航空学报, 2017, 38: 260
9 Tian J Q. The electrochemical corrosion behavior of tungsten-aluminum (W-Al) alloy in NaCl solution [D]. Qingdao: Ocean University of China, 2013
9 田继强. 钨铝合金在NaCI溶液中的电化学腐蚀行为研究 [D]. 青岛: 中国海洋大学, 2013
10 Shao H B, Zhang J Q, Wang J M, et al. EIS analysis on the anodic dissolution process of pure aluminum in an alkaline solution [J]. Acta Phys. Chim. Sin., 2003, 19: 372
10 邵海波, 张鉴清, 王建明等. 纯铝在强碱溶液中阳极溶解的电化学阻抗谱解析 [J]. 物理化学学报, 2003, 19: 372
11 Real S, Urquidi-MaCdonald M, MaCdonald D D. Evaluation of alloy anodes for aluminum-air batteries [J]. Cheminform, 1988, 20: 2410
12 Wang J B. Corrosion and electrochemical behavior of aluminum in alkaline media [D]. Hangzhou: Zhejiang University, 2008
12 王俊波. 铝在碱性介质中的腐蚀与电化学行为 [D]. 杭州: 浙江大学, 2008
13 Liu Y Q, Li G M, Chen S, et al. Influences of copper ions and potential on cathodic protection behaviors of aluminum alloy 5083 [J]. Mater. Prot., 2017, 50(5): 88
13 刘亚强, 李国明, 陈珊等. 铜离子及电位对5083铝合金阴极保护行为的影响 [J]. 材料保护, 2017, 50(5): 88
14 Harrington S P, Devine T M. Relation between the semiconducting properties of a passive film and reduction reaction rates [J]. J. Electrochem. Soc., 2009, 156(4): C154
15 Song W H. The study on the dependence of corrosion process of magnesium anodic films on pH [D]. Chongqing: Chongqing University, 2012
15 宋卫华. 镁合金阳极氧化膜的腐蚀过程随pH变化的研究 [D]. 重庆: 重庆大学, 2012
16 Zhao X H. Study of electrochemical impedance spectroscopy on anodized aluminum alloys [D]. Beijing: Beijing University of Chemical Technology, 2016
16 赵旭辉. 铝阳极氧化膜的电化学阻抗特征研究 [D]. 北京: 北京化工大学, 2016
17 Lv Y L. Steam turbine rotor thermal embrittlement detection method based-on electrochemical impedance spectroscopy [D]. Beijing: North China Electric Power University (Beijing), 2016
17 吕亚玲. 基于电化学阻抗谱的汽轮机转子钢热脆化检测方法研究 [D]. 北京: 华北电力大学 (北京), 2016
18 Hu B. The corrosion inhibition of rare passivation and the corrosion behavior of 7075 aluminum alloy in alkaline solution with NaCl [D]. Xining: Qinghai Normal University, 2014
18 胡博. 7075型铝合金在碱性NaCl介质中的腐蚀行为及稀土钝化缓蚀作用 [D]. 西宁: 青海师范大学, 2014
19 Hu B, Wang J C, Liu Y, et al. The corrosion behavior of 7075 al alloy in alkaline NaCl [J]. Mater. Prot., 2014, 47(3): 23
19 胡博, 王建朝, 刘影等. 7075型铝合金在含NaOH碱性NaCl溶液中的腐蚀行为 [J]. 材料保护, 2014, 47(3): 23
20 Sheng H, Dong C F, Xiao K, et al. Effect of pH on electrochemical behavior of 2024-T351 aluminium Alloy in NaCl solution [J]. Corros. Prot., 2013, 34: 107
20 生海, 董超芳, 肖葵等. pH值对2024-T351铝合金在NaCl溶液中电化学行为的影响 [J]. 腐蚀与防护, 2013, 34: 107
21 Chen Y L, Wang A D, Bian G X, et al. Study on electrochemical behavior of 2024-T3 aluminum alloy in different acidic aqueous solutions [J]. Failure Anal. Prev., 2017, 12: 78
21 陈跃良, 王安东, 卞贵学等. 2024-T3铝合金在不同酸性水溶液中的电化学行为 [J]. 失效分析与预防, 2017, 12: 78
22 Moon S M, Pyun S I. Faradaic reactions and their effects on dissolution of the natural oxide film on pure aluminum during cathodic polarization in aqueous solutions [J]. Corrosion, 1998, 54: 546
23 Cao C N, Wang J, Lin H C. Effect of Cl- ion on the impedance of passive-film-covered electrodes [J]. J. Chin. Soc. Corros. Prot., 1989, 9: 261
23 曹楚南, 王佳, 林海潮. 氯离子对钝态金属电极阻抗频谱的影响 [J]. 中国腐蚀与防护学报, 1989, 9: 261
24 Ma J L, Wen J B, Lu X W, et al. Electrochemical impedance spectroscopy of aluminum alloy anode during corrosion process [J]. Corros. Prot., 2009, 30: 373
24 马景灵, 文九巴, 卢现稳等. 铝合金阳极腐蚀过程的电化学阻抗谱研究 [J]. 腐蚀与防护, 2009, 30: 373
25 An B G, Zhang X Y, Song S Z, et al. A study of electrochemical impedance spectrum for corrosion behavior of LY12 aluminum alloy in simulated acid rain [J]. J. Chin. Soc. Corros. Prot., 2003, 23(3): 167
25 安百刚, 张学元, 宋诗哲等. LY12铝合金在模拟酸雨溶液中的阻抗谱研究 [J]. 中国腐蚀与防护学报, 2003, 23(3): 167
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





