沿海地区服役的飞机经常遭受高盐雾、高湿度等因素的影响,易发生海洋环境下的大气腐蚀 。飞机蒙皮、大梁、桁条等铝合金材料结构件已成为腐蚀的多发区 。腐蚀失效降低铝合金力学性能,影响飞机结构完整性,进而威胁飞行安全。
高湿度的海洋大气环境下,铝合金表面沉积的无机盐(主要为 NaCl)吸附、凝聚空气中的水分,促进薄液膜的形成与扩展。铝合金大气腐蚀主要是在薄液膜下的电化学腐蚀 ,与溶液中的腐蚀有很大区别,这主要是由于薄液膜厚度的变化影响了电极反应的传质过程,如溶解氧的扩散、腐蚀产物的积聚等 ,进而对大气腐蚀的速率产生显著的影响 。薄液膜厚度均在微米级别,一般采用扫描开尔文探针技术(Scanning Kelvin Probe,SKP)研究金属在薄液膜下的腐蚀行为,但 SKP 技术并不成熟且测量过程中探针的振动会使液膜产生对流效应,加速 O 2 在液膜中的扩散,影响测量的准确性 。目前,国内多采用传统的电化学方法研究薄液膜下的金属腐蚀行为,液膜厚度由前端装有尖端铂丝(或其他稳定金属)的千分尺、欧姆表(或电池、电流表)构成的装置测量 。薄液膜下铝合金的腐蚀行为研究多采用阴极极化和电化学阻抗谱法(Electrochemical Im-pedance Spectroscopy,EIS) ,而对与腐蚀有关的阳极极化行为鲜有研究报道。
本研究以飞机承力结构使用的 7B04 铝合金作为研究对象,模拟海洋大气环境,建立并验证盐沉积量、相对湿度与薄液膜厚度之间的关系,搭建能控制薄液膜厚度的电化学测试装置,采用动电位极化测量方法研究7B04 铝合金在不同厚度及不同 NaCl 浓度液膜下的腐蚀电化学行为。
1 实验
1. 1 实验材料
7B04 铝合金板材由东北轻合金有限责任公司生产,其化学成分见表 1。

1. 2 薄液膜电化学测试装置
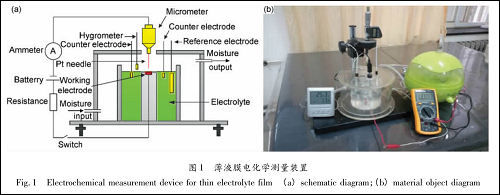
薄液膜的厚度与空气相对湿度密切相关,文献中的测试装置均在大气环境下测量,可能会由于湿度较低导致溶液蒸发较快,引起薄液膜厚度的不断变化,影响测量准确度。为此,参考李亚坤等 的设计在测试装置外加装了环境湿度控制装置,如图 1 所示。装置内加装高灵敏度温湿度计,通过控制从加湿器输入的湿气量来调节测量装置内的相对湿度,实验温度为(25 ± 0. 2)℃的室温;试样测量面大小选择为 10 mm × 10 mm,打磨抛光成平整的镜面,使试样表面液膜厚度保持均匀、稳定。
液膜厚度测量装置采用的千分尺精度为 1 μm,前端安装铂针,测量回路串联有电池、电阻及高灵敏度电流表。进行厚度测量时,转动千分尺使铂针下移,一旦铂针与液膜接触,电流会发生突变,而当铂针接触到铝合金表面时电流又有一突变,两次电流突变间铂针移动的距离即为液膜厚度。
1. 3 电化学实验
将 7B04 铝合金板切割加工成尺寸为 10 mm ×10 mm × 3 mm 的电极,用直径 3 cm 的 PVC 管固定,预留 1 cm 2 的测试面,其余面均用环氧树脂封装。测试面采用水磨砂纸逐级打磨至 3 000 # ,经金刚石研磨膏抛光,丙酮和无水乙醇除油、除水后,安装至薄液膜电化学测量装置。采用动电位扫描法测量极化曲线,扫描速率为 1 mV/s。
电化学测量设备为 PARSTAT 4000 电化学综合测试仪,电解池为三电极体系,参比电极为饱和甘汞电极(Saturated Calomel Electrode,SCE),对电极为两个铂片电极,安放位置如图 1 所示。
2 薄液膜厚度的确定
2. 1 薄液膜厚度的理论计算
若金属表面不均匀或沉积有固体颗粒,则水蒸气优先在表面上的这些活性部位发生凝聚或吸附,进而长大成主液滴,经一系列连续过程,在金属表面形成薄液膜。在一定温度下,薄液膜稳定后与周围水蒸气构成气-液二相平衡体系,水蒸气分压和液相组成一一对应 。大气相对湿度由水蒸气分压确定,文献给出了大气相对湿度与 NaCl 溶液液相组成之间的关系。20 ~25 ℃下,溶液中 NaCl的质量分数与大气相对湿度的关系及多项式拟合公式如图 2 所示。
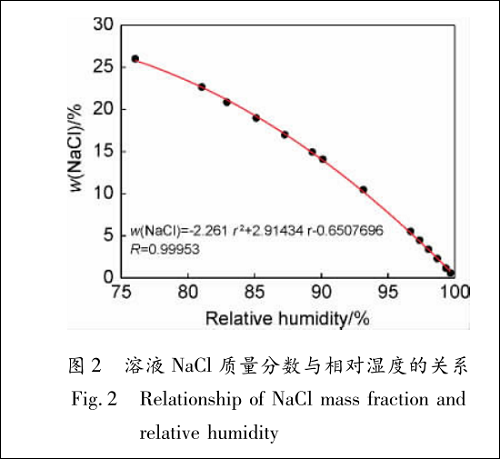
图 2 拟合公式中 r 为大气相对湿度,% 。20 ~25 ℃下,NaCl 与其饱和溶液(质量分数为 26% )平衡的相对湿度为 76% 左右,只有环境相对湿度≥76% ,NaCl 颗粒才能吸收环境水汽而潮解,在铝合金表面形成液膜,从而诱发腐蚀过程,故由图2 拟合的公式仅适用于 r≥76% 。随着相对湿度的不断增加,薄液膜吸水导致 NaCl 溶液浓度降低。不同浓度的 NaCl 溶液密度由 OLI Analyzer 软件计算获得,结合图 2 数据整理后获得 NaCl 溶液密度与大气相对湿度的关系及多项式拟合公式,如图 3所示。
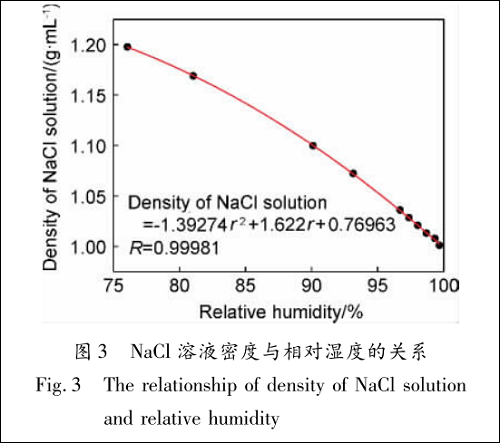
假设薄液膜中的 NaCl 全部来源于铝合金表面的 NaCl 沉积,因此可得到如下关系:
ρ·h·s = d·s (1)
式中: ρ 为溶液密度,g/mL; h 为薄液膜厚度,cm; s为铝合金表面积,cm 2 ; d 为铝合金表面 NaCl 沉积量,g/cm 2 。故薄液膜厚度可以表示为:
h = d/ρ (2)
将图 2 与图 3 中的多项式拟合公式带入(2)式,获得薄液膜厚度与大气相对湿度(r≥76%)、铝合金表面 NaCl 沉积量的关系式:
![]()
由(3)式计算的薄液膜厚度数据与文献推导的关系式计算值基本一致,该计算结果已被应用到其他大气腐蚀研究中 ,但目前仍缺乏该关系式的实验验证报道。
2. 2 薄液膜厚度的测量与验证
某两个海域实验场的氯离子平均沉降量分别为60 mg/dm 2 和 21. 9 mg/dm 2,假设氯离子全部来源于 NaCl 沉积,将氯离子沉积量折算为 NaCl 沉降量:9. 89 ×10-4g/cm 2 和 3. 61 ×10-4 g/cm 2 。
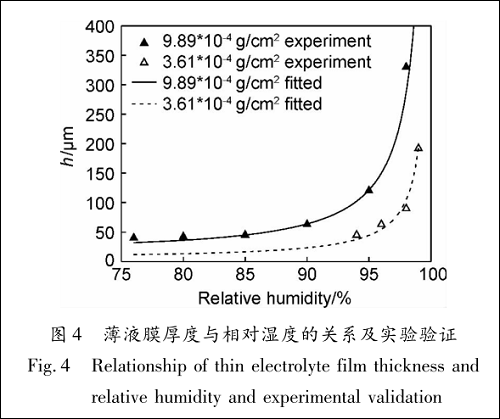
使用微量滴管向面积为1 cm 2 的 7B04 铝合金电极表面滴加质量分数为 3. 5% 的 NaCl 溶液,干燥后NaCl 均匀沉积在电极表面,重复几次最终使电极表面NaCl 沉积量分别为9.89 ×10-4 g 和3.61 ×10-4 g。将电极置于电化学测量装置内(不加溶液),按照图 1连接好测量线路,通过加湿器调节装置的相对湿度,当相对湿度达到76%时,NaCl 开始吸水溶解成液膜。 转动千分尺测量液膜厚度,当薄液膜厚度大于 30 μm时,薄液膜厚度测量数据趋于稳定且重现性较好,薄液膜厚度与大气相对湿度的关系及测量数据结果见图4,与拟合曲线吻合较好,说明拟合的薄液膜厚度与大气相对湿度的关系曲线和实验结果相符。
3 7B04 铝合金在薄液膜下的腐蚀电化学行为
3. 1 薄液膜对 7B04 铝合金自然腐蚀电位的影响
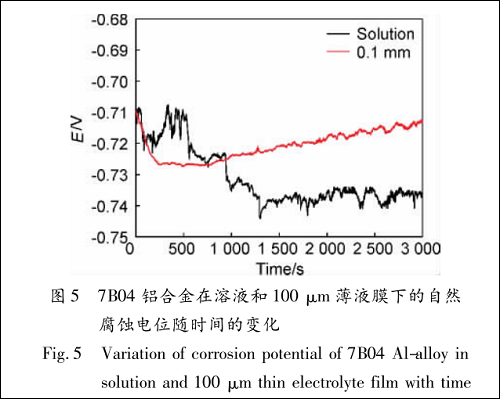
在质量分数为 3. 5% 的 NaCl 本体溶液及相同浓度的 100 μm 薄液膜下,分别测量 7B04 铝合金自然腐蚀电位随时间的变化,结果如图 5 所示。从图5 可以看出,薄液膜下 7B04 铝合金的自然腐蚀电位相对较正,这与不锈钢的 SKP 测量结果趋势相同 。7B04 铝合金自然腐蚀电位在溶液中需要1400 s 才达到稳定,而在 100 μm 液膜下只需 250 s左右即达到稳定,说明薄液膜下氧气扩散速率快,电极表面阴阳极反应很快即达到平衡。随着腐蚀的进行,腐蚀产物在薄液膜下不易扩散产生积聚,导致自然腐蚀电位在 800 s 后呈上升状态,而溶液中的腐蚀产物扩散条件好,故自然腐蚀电位比较稳定。
3. 2 薄液膜厚度对 7B04 铝合金腐蚀电化学行为的影响
由式(3)可知,在相对湿度恒定的情况下,盐沉积量与薄液膜厚度成正比,故盐沉积量和薄液膜厚度一一对应,二者对 7B04 铝合金腐蚀电化学行为的影响相一致。
将处理好的 7B04 铝合金电极安装于薄液膜电化学测量装置中,周围添加质量分数为 3. 5% 的NaCl 溶液,将装置相对湿度控制在 98% (据图 2),通过微量吸管调整电极表面液膜厚度(同时模拟了不同的盐沉积量),待气液两相达到平衡、液面稳定后再测量 7B04 铝合金电极的电化学行为,不同厚度液膜下的极化曲线测量结果如图 6 所示。
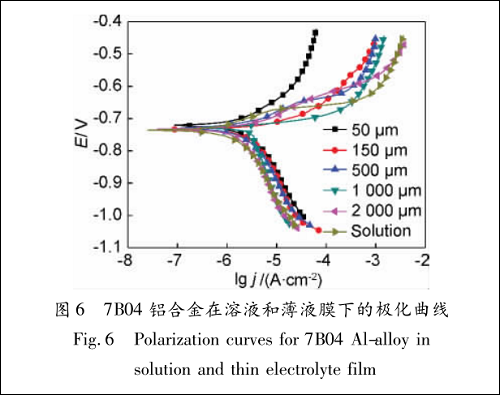
从图 6 可以发现,7B04 铝合金在液膜下的自然腐蚀电位均比本体溶液中稍高,其自然腐蚀电位分布在 -0. 74 ~ -0. 72 mV 之间。7B04 铝合金的阴极极化主要为 O 2 的还原反应,受 O 2 的扩散过程控制,液膜越薄,O 2 扩散速率越快。当薄液膜厚度≤100 μm 时,电极表面的扩散层即为液膜 ,O2 不经过本体溶液的扩散即可到达电极表面扩散层,提高了 O 2 的还原速率,在阴极极化曲线上表现为:随着液膜厚度的减小,阴极极化电流密度不断增加,而当液膜厚度为 1000 μm 和 2000 μm 时,阴极极化行为已呈现本体溶液的特征,其阴极极化曲线与本体溶液中相差无几。
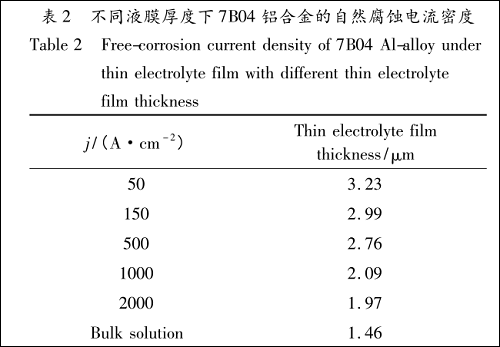
O 2 的还原速率的提高导致在自然腐蚀状态下,液膜越薄,自然腐蚀电流密度(腐蚀速率)也越大(见表 2),50 μm 薄液膜下 7B04 铝合金的自然腐蚀速率相当于本体溶液中的 2 倍多。但随着腐蚀的进行,腐蚀产物积聚在电极表面无法扩散,阳极反应受到抑制,故在阳极极化曲线上可以看到:随着极化电位的升高,液膜厚度越小其阳极极化电流密度也越小,说明液膜越薄,腐蚀产物越容易积聚,也越容易抑制阳极反应过程。图 7 为阳极极化后电极表面放大 20 倍的腐蚀形貌图,相对于本体溶液中的腐蚀,薄液膜下的 7B04 铝合金腐蚀更轻,且表现出不均匀的局部腐蚀特征,腐蚀主要出现在边缘及中间不确定位置,这主要是由于薄液膜下电极表面电流分布不均造成的。

3. 3 薄液膜 NaCl 浓度对 7B04 铝合金腐蚀电化学行为的影响
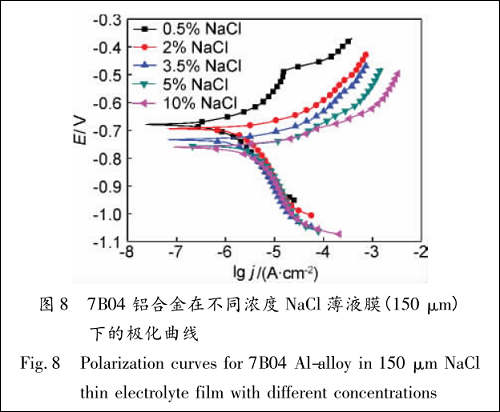
大气相对湿度调节着 7B04 铝合金表面薄液膜的 NaCl 浓度,相对湿度越大,NaCl 浓度越小。 结合图 2,改变薄液膜电化学测量装置的相对湿度,电极周围添加相应浓度的 NaCl 溶液,通过微量吸管将电极表面薄液膜厚度均调整为 150 μm,测量不同条件下 7B04 铝合金的极化曲线,结果如图 8 所示。
图 8 显示,随着 NaCl 浓度的增加,7B04 铝合金的自然腐蚀电位降低,这与 AA5083 铝合金在不同NaCl 浓度下的自然腐蚀电位 SKP 测量结果趋势相一致 。从图 8 中还可以看出,NaCl 浓度增加,自然腐蚀电流密度上升,NaCl 质量分数为 5% 和 10%时,二者自然腐蚀电位与自然腐蚀电流相差不大,说明铝合金表面钝化膜的 Cl-吸附量有限,当达到平衡后铝合金的自然腐蚀电位基本不变。阴极极化曲线基本一致,说明阴极极化过程受到 NaCl 浓度变化影响不大;阳极极化电流密度随 NaCl 浓度的增加而有所增大,但较本体溶液中的腐蚀要轻,说明阳极反应均受到了抑制。
4 结论
(1)7B04 铝合金表面的薄液膜厚度与盐沉积量和大气相对湿度有关,拟合建立了三者之间的关系式,采用搭建的电化学测量装置测量了不同盐沉积量和相对湿度下的薄液膜厚度,测量结果与计算结果基本相符。
(2)薄液膜下7B04 铝合金的自然腐蚀电位较本体溶液中稍正,自然腐蚀电流密度(腐蚀速率)更大,50 μm 薄液膜下的自然腐蚀电流密度相当于本体溶液中的2 倍多,自然腐蚀电位到达稳定的时间更短,但由于腐蚀产物在薄液膜下不易扩散产生积聚,导致自然腐蚀电位在稳定一段时间后呈上升状态。
(3)随着薄液膜厚度的减小,O 2 扩散速率加快,7B04 铝合金阴极极化电流密度增加,而腐蚀产物积聚在薄液膜下,导致阳极反应受到抑制,减缓了腐蚀。
(4)随着薄液膜中 NaCl 浓度的升高,7B04 铝合金的自然腐蚀电位降低,自然腐蚀电流密度上升,当NaCl 质量分数达到5%后,自然腐蚀电位基本不再变化,而阴极极化过程受 NaCl 浓度变化影响不大,阳极极化电流密度有所增加,但仍然受到抑制,腐蚀较轻。
更多关于材料方面、材料腐蚀控制、材料科普等方面的国内外最新动态,我们网站会不断更新。希望大家一直关注中国腐蚀与防护网http://www.ecorr.org
责任编辑:殷鹏飞
投稿联系:编辑部
电话:010-62313558-806
中国腐蚀与防护网官方 QQ群:140808414
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





