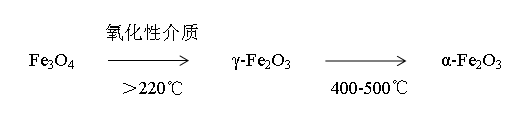01 铁-氧平衡图与氧化层结构
氧在铁中的溶解度很低,汤根斯(Tankins)等人测定在体心立方铁中氧的溶解度为:
Log[O%]=-126330/T+5.51
在常温下α-Fe溶氧量小于0.05%,在950℃时溶氧量约0.2%,可形成含氧的固溶体。它比纯铁更具有正的化学电位,从-0.43伏到零。
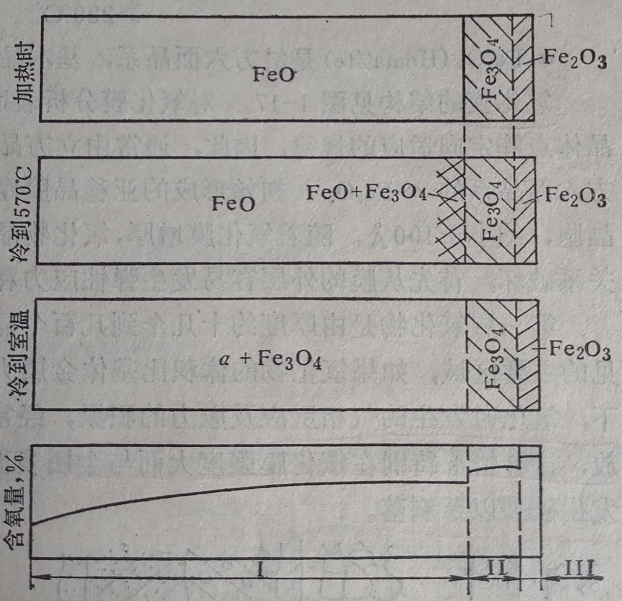
图1 铁氧平衡图
图1为铁-氧平衡图。氧与铁形成不同结构的氧化膜组成相,由平衡图上可看出依含氧量不同分别为FeO(FexO)、Fe3O4、Fe2O3。铁的氧化物相的含氧量见表1,它们在表面的分布见图2所示。
表1 不同氧化物相的成分
图2 氧浓度在铁表面的分布及各相结构
FeO又称维氏体(Wustite),是具有岩盐型的立方点阵的缺位固溶体,过剩的氧在FeO中以氧离子形态存在并占据晶格的阴离子结点。由于氧在FeO固溶体中有一个固溶范围,如在1000℃时,Fe:O=1:1.05-1.14,相当于Fe0.95O-Fe0.88O(含氧的原子百分数为51.2-53.3%),所以也可写成FexO的通用形式。
高温氧化皮中的FeO是介稳状态,低温下它将分解。
Fe3O4,又称磁性氧化铁,具有尖晶石型点阵,它从室温到1583℃都是稳定的,在氧化性介质中加热时,将失去磁性。
2Fe3O4+1/2O2→3Fe2O3
α-Fe2O3是斜方六面晶系,基本晶胞由4个Fe3+与6个O-结合而成。
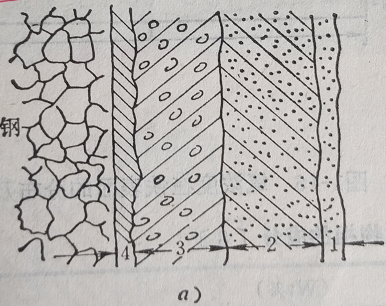
图3 氧化膜的结构
a)铁的氧化膜结构
b)多晶体表面开始形成的亚稳晶膜
1-Fe2O3;2-Fe3O4
3-FeO+Fe3O4;4-FeO
氧化膜的结构见图3所示。对氧化膜分析表明,与基体金属相连的第一层氧化物,遵循晶体点阵定向适应的规律,因此,通常由立方晶系的Fe3O4、γ-Fe2O3或FeO组成,而不是斜方六面晶系的α-Fe2O3。初始形成的亚稳晶膜厚度极小,从单分子吸附层到几个定向氧化物晶胞,约小于100?。随着氧化膜增厚,氧化物晶格中累积的弹性应力使膜与基底的定向适应关系破坏,首先从膜的外层容易发生弹性应力释放,同时氧化膜内晶体发生再结晶。
图4 产品氧化案例
第一层氧化物是由厚度约十几个到几百个晶胞所构成,在该层的外边形成的氧化膜是可见的主要区域,如果氧化物的体积比基体金属大时,在氧化膜中存在着残余压应力。在高温下氧化时发生的气相反应及应力的积累,经常使氧化皮下产生突起的小泡而使应力部分释放,这种情况特别在氧化膜强度大而金属表面附着力又很弱时容易出现,并经常使氧化膜发生破裂以致剥落。(注:这里解释了产品严重氧化时表面氧化皮脱落的原因,可以重点记一下。)
02 氧化膜形成的机理
氧化膜的发展和形成的过程比较复杂,因此开始形成氧化膜时就将介质和金属基体分隔开来,进一步氧化必须通过这个氧化物层。
显然氧化过程是由金属、金属氧化物和氧三者之间的相互作用和氧的扩散所控制。在大多数情况下,离子或电子迁移速率控制着氧化速率,但有时界面反应也是控制氧化速率的决定因素。
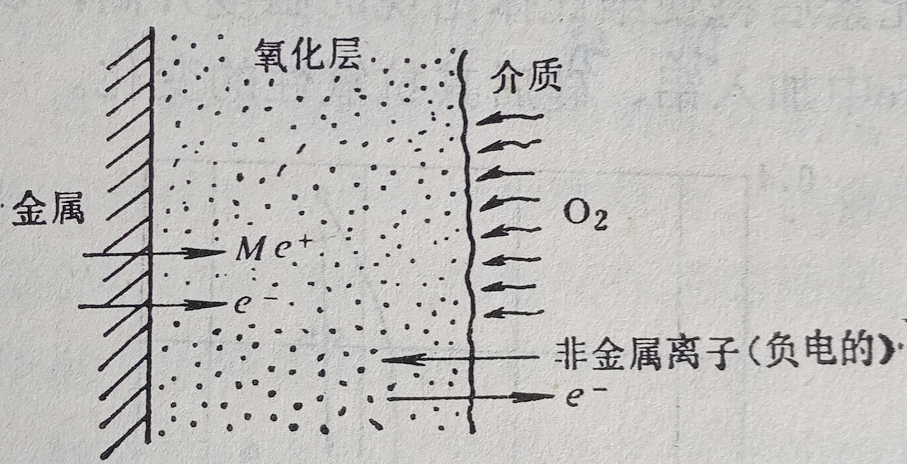
图5 金属表面与氧化介质间的作用
在图5中表示氧以负离子状态被吸附在氧化层表面上,而金属以正离子状态溶解在氧化膜中,所以氧化过程的推动力是浓度梯度(dc/dx)和氧化层中的电场。其中电场是由于在边界上的电子与离子运动速度不一样,从而形成双电荷层而产生的。
图6 铁的表面氧化机理示意图
铁的氧化机理可以从离子-电子在界面上的迁移过程来说明(图6所示)。
1)首先,在界面Ⅰ上的铁原子形成Fe2+与2e-,并向FeO层中扩散,同时使界面Ⅰ向铁的一侧内移。
2)在界面Ⅱ上,FeO层中的Fe2+与来自Fe3O4层中的O-生成FeO晶格,与此同时一部分Fe2+从界面Ⅱ向Fe3O4方向扩散。
3)在界面Ⅲ的Fe3O4一侧,按Fe2+(FeO)+2Fe3+(Fe2O3)+4O-(Fe2O3)→Fe3O4反应形成Fe3O4,此外,在界面Ⅲ的Fe2O3一侧,按2Fe3+(Fe3O4)+6O-(Fe2O3)→Fe2O3反应形成Fe2O3。
4)在最表层Ⅳ上,O2吸附在Fe2O3表层,在Fe2O3层中O-向界面Ⅲ方向移动;由于形成速度慢,Fe2O3层很薄。
在高温下氧化,由于氧化层中的压应力及CO2气体反应使氧化层发生龟裂及剥落,O2沿缝隙迅速侵入金属内层使氧化速度急剧上升。
03 影响因素
氧化膜的形成速度主要与介质成分、加热温度及保温时间、钢材的成分等因素有关。
1 钢成分的影响
图7是碳钢高温氧化的速度与含碳量的关系。
图7 碳钢含碳量与高温氧化速度的关系
当含碳量小于0.04%时,氧化速度随含碳量增长而升高;当含碳量大于0.4%时,氧化速度却随含碳量增加而减小。显然是由于氧化介质与钢中的碳相互作用形成气体CO、CO2有关。
图8 铁铝合金氧化烧损与温度的关系
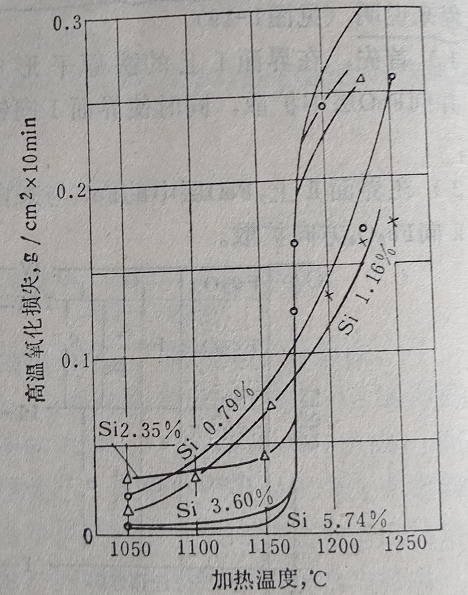
合金元素对氧化速度有很大影响,加入铬、铝、硅等元素可以形成致密的尖晶石型氧化物(Cr2O3、Al2O3、SiO2),这种氧化物结构对离子扩散有强烈的阻止作用,同时铁中添加合金元素后将使维氏体出现的温度升高,以致抗氧化能力大大提高,见图8、图9。表明Fe中加入铝、硅后其抗氧化的变化。
图9 铁硅合金的氧化烧损与加热温度的关系
2 加热温度与时间的影响
瓦格纳(Wagner)指出,在加热初期氧化层很薄时(<100?)界面双电场作用强,界面迁移速度一方面取决于浓度梯度dc/dx,另一方面又取决于电场强度。此时,氧化层厚度与温度间呈下列关系:
X1/X=A-Inτ
式中:X1-系数(10-4-10-5cm),X-时间τ时的氧化层厚度,A-常数,τ-时间,上式是在薄层氧化时(氧化层厚度<100?)氧化膜成长的对数定律。
当氧化层厚时,氧化速率与层的厚度成反比,此时氧化层的增长速度服从抛物线定律:
X=Aτ1/2
图10为纯铁在空气中加热时保温时间与氧化层厚度的关系。
图10 纯铁在空气中加热时保温时间与氧化膜厚度的关系
氧的扩散系数与温度呈指数关系,因此,氧化膜的增厚随加热温度升高也呈指数曲线上升。
图11 含碳0.60%钢加热温度与氧化速度的关系
图11是含碳0.6%钢氧化温度与氧化速度(用5小时内氧化皮增重表示)的关系。
04 结束语
氧化,是产品出现的比较严重的表面腐蚀现象。了解了它生成的原理,对于我们后续采取相应措施,能起到一定的指导作用。
好的,本期文章到此就结束了,欲知后续精彩内容,且看下期分解。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。
相关文章

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808414
点击排行
PPT新闻
“海洋金属”——钛合金在舰船的
点击数:8181
腐蚀与“海上丝绸之路”
点击数:6497