肖涛1,2 Masoumeh Moradi2 宋振纶2 杨丽景2 闫涛1,2 侯利锋1
1. 太原理工大学材料科学与工程学院太原030024;2. 中国科学院宁波材料技术与工程研究所中国科学院海洋新材料与应用技术重点实验室宁波315201
1 前言
碳钢被广泛应用于石油工业、建筑、工程结构及海洋环境中。在酸性条件下,会发生电化学腐蚀[1],造成大量的经济损失。为抑制酸性环境对碳钢的腐蚀,加入缓蚀剂是一种简单而有效的办法[2]。然而,大部分缓蚀剂对人类和环境都有害[3]。因此,应选择成本低廉、对环境友好的绿色缓蚀剂。草药提取物、水果萃取物等取自天然植物的聚合物由于其内部结构的稳定性成为一类较为重要的缓蚀剂[4],然而大部分价格昂贵,使其应用受到限制。细菌胞外聚合物(EPS) 是一种含多糖、蛋白质、核酸、脂类和其他高分子的天然聚合物[5]。因EPS 结构、物理、流变性及其他特性的多样性,广泛应用于食品和乳制品工业。已有报道[6]表明,EPS由于其官能团的作用可吸附在金属表面形成较为致密的保护膜。
弧菌是一种广泛存在于海洋生态系统中且能形成生物膜的微生物[7],并且来自该弧菌的EPS 制备过程简易、成本低、无毒、对环境污染小、高效且可再生[8],是一种绿色缓蚀剂。本文采用新喀里多尼亚弧菌EPS 作为缓蚀剂,研究其在0.5 mol/LH2SO4溶液中对Q235碳钢的缓蚀作用。
2 实验方法
2.1 实验材料
实验材料为Q235钢,试样尺寸为15mm×15mm×4 mm。其化学成分(质量分数,%) 为:C 0.2,Mn1.4,Si 0.35,S 0.045,P 0.045,Fe 余量。Q235 钢用金刚石砂纸从400,600,1000,1500 和2000#逐级打磨光滑,酒精中超声清洗,吹干备用。实验介质为人造海水,成分(mol/L) 为:NaCl 0.42,Na2SO4 0.029,KCl 0.009,KBr 0.1,MgCl2·6H2O 0.055,GaCl2 0.01,H3BO3 0.005,NaHCO3 0.002,其余为蒸馏水。新喀里多尼亚弧菌EPS 的制备如下:人造海水1 L、鱼粉蛋白胨5 g/L、酵母膏1 g/L、葡萄糖30 g/L。120 ℃下灭菌20 min,冷却后紫外灭菌1 h。然后加入细菌,置于28 ℃的震荡培养箱中以130 r/min 的速度震荡培养3 d。完成后在4 ℃以1.35×104 g 的速度离心15 min。上层溶液用0.22 μm的密理博过滤器过滤,然后加入所得滤液3 倍体积的异丙醇,配置为悬浊液。将悬浊液放入0 ℃冰箱24 h 使固体充分析出,在常温下以7×103 g 的速度离心5 min。除去上层清液,所得固体即为EPS。
2.2 测试方法
电化学阻抗和极化曲线测量使用(PGSTAT302,Autolab) 电化学工作站,采用三电极体系,辅助电极为Pt 电极,参比电极为饱和KCl甘汞电极,工作电极为Q235 钢,面积为2.25 cm2,非工作面用环氧树脂封装。电解液为添加或未添加EPS 的0.5 mol/L H2SO4溶液。电化学阻抗测试扰动电位幅值为±10 mV,扫描频率从105~10-2 Hz。极化测试扫描范围为相对于开路电位?00 mV,扫描速率为0.2 mV/s。所有电化学测试都在体系稳定20 min 后进行,电化学测试溶液和环境温度均为25 ℃。
Fourier 转换红外吸收光谱(FT-IR) 测试采用KBr 压片法进行(NICOLET 6700,Thermo),扫描范围为4000~500 cm-1。Q235 钢在未添加或添加EPS的0.5 mol/L H2SO4溶液中分别浸泡2 h,N2吹干。腐蚀形貌使用扫描电子显微镜(SEM,Quanta FEG250,FEI) 进行观察。
3 结果与讨论
3.1 电化学阻抗
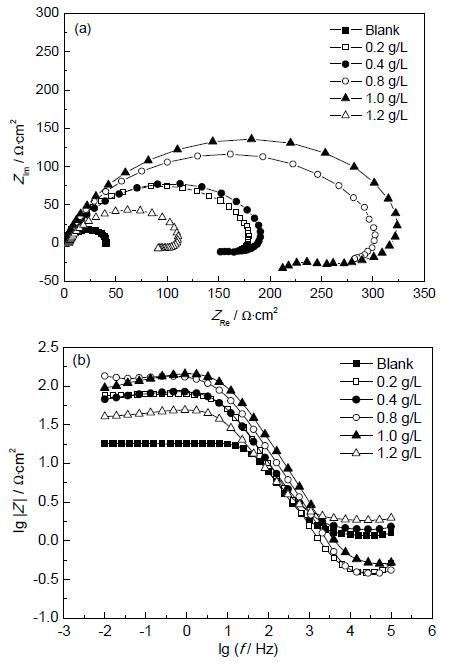
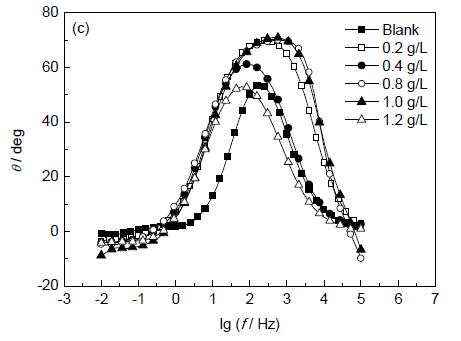
图1 Q235 钢在含不同浓度EPS 的0.5 mol/L H2SO4溶液中的电化学阻抗谱
Fig.1 Nyquist (a) and Bode (b, c) plots for Q235 steel immersedin 0.5 mol/L H2SO4 solutions with variousconcentrations of EPS
图1 为Q235 钢在含不同浓度EPS 的0.5 mol/LH2SO4溶液中的电化学阻抗谱。从图中可以看出,阻抗弧由高频区的容抗弧和低频区的感抗弧组成。通常认为,阻抗谱的高频容抗弧象征着电极表面和溶液间的双电层弛豫过程[9]。阻抗谱的高频容抗弧直径反映了电荷转移电阻Rct的大小,Rct的倒数正比于腐蚀速率的大小。容抗弧模值大,则反应阻力大,阳极的腐蚀速率慢。而感抗弧是由于金属表面吸附如FeSO4或者缓蚀剂等物质的弛豫过程,或者是由于钝化膜的溶解[10]。从图1 可以看出,添加EPS 后,Rct增加,说明EPS 能够抑制电子从碳钢表面向溶液转移,抑制了碳钢的腐蚀。从图中还可以看出,Rct与EPS 的浓度有关,随着EPS 浓度的增加,Rct不断增大。从Bode 图可看出,随EPS 浓度的增加,缓蚀效率增加。从相位图可知,加入EPS后,相位图幅度变大,并且向高频移动,说明在碳钢表面形成了一层较为致密的膜层。EPS 对Q235 钢的缓蚀与EPS 在碳钢表面的覆盖率θ有关,θ越大,对碳钢的缓蚀效率越好。当EPS 浓度增加到1.0 g/L 时,Rct值达到最大,意味着θ达到最大。当EPS 浓度超过1.0 g/L 后,Rct反而减小。电化学阻抗拟合参数列于表1,缓蚀率η通过下式计算得出:
η = (Rct -R0ct)/Rct ×100% (1)
式中,Rct为添加EPS 时碳钢表面的电荷转移电阻;Rct0为未添加EPS时碳钢表面的电荷转移电阻。
对阻抗谱进行拟合所用的等效电路见图2。其中,图2a 为未加入EPS 时的等效电路,图2b 为加入EPS 的等效电路。Rs为溶液电阻,Rct和Q 分别表示电荷转移电阻和双电层电容,L 表示感抗,RL表示感抗电阻。
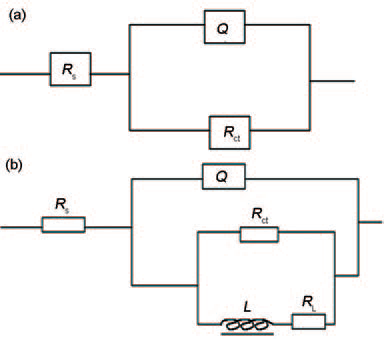
图2 未加入EPS和加入EPS的EIS 等效电路
Fig.2 Equivalent circuit models of EIS in 0.5 mol/LH2SO4 solutions without (a) and with (b) EPS
EPS在Q235 钢表面的覆盖率θ通过下式计算得出[11,12]:
(1-θ)= R0ct/Rct(2)
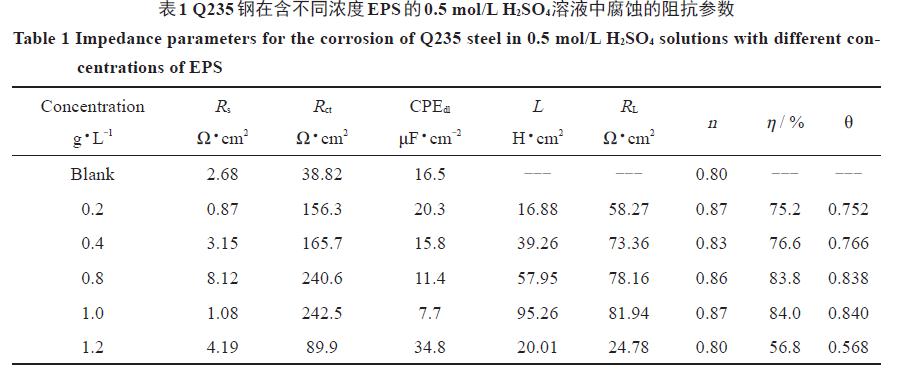
从表1 可以看出,随着EPS 浓度的增加,Rct 和θ 增大,缓蚀率也逐渐增大。Rct 从未添加EPS 时的38.82 Ω·cm2 增加到添加1.0 g/L EPS 时的242.5 Ω·cm2,θ达0.840,此时缓蚀率达到最大值,为84.0%。当继续增大EPS 浓度时,Rct和θ减小,缓蚀率减小。而电容随EPS 浓度的增加而减小,感抗随EPS 浓度的增加而增大,都是由于EPS 是一种大分子物质,吸附在碳钢表面后,形成一层较为致密的膜层,能阻碍腐蚀性溶液与碳钢的接触。感抗随EPS浓度的增加而增大也说明了EPS在碳钢表面的吸附未达到吸附-脱附动态平衡过程,此时以吸附为主。当EPS 浓度达到1.2 g/L 时,感抗减小,则是由于过多的EPS 吸附溶液中的Fe3+,加速阳极金属的溶解,导致膜层溶解,破坏了膜层的致密性,从而降低了EPS对碳钢的缓蚀作用。
3.2 极化曲线
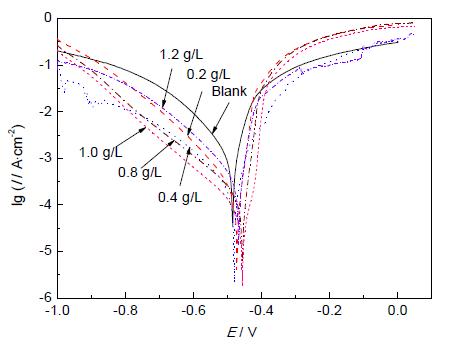
图3 Q235 钢在含不同浓度EPS 的0.5 mol/L H2SO4溶液中的极化曲线
Fig.3 Polarization curves for Q235 steel immersed in0.5 mol/L H2SO4 solutions with various concentrationsof EPS
图3 为Q235 钢在含不同浓度EPS 的0.5 mol/LH2SO4 溶液中的极化曲线。可以看出,当添加EPS后,Q235 钢在0.5 mol/L H2SO4溶液中的极化曲线有着明显的变化。随EPS浓度的增加,腐蚀电位正移,腐蚀电流密度下降,说明EPS 的加入抑制了硫酸对Q235 钢的腐蚀。当EPS浓度达到1.0 g/L 时,其腐蚀电流密度达到最小。当其浓度达到1.2 g/L 时,曲线上升,腐蚀电流密度增大,说明在0.5 mol/L H2SO4溶液中EPS 对Q235 钢的最佳缓蚀浓度为1.0 g/L。其拟合得出的动电位极化参数列于表2。缓蚀率通过下式计算得出:
η = (I 0corr -Icorr)/I 0corr(3)
式中,I 0corr 为未添加EPS时的极化电流密度;Icorr为添加EPS后的极化电流密度。
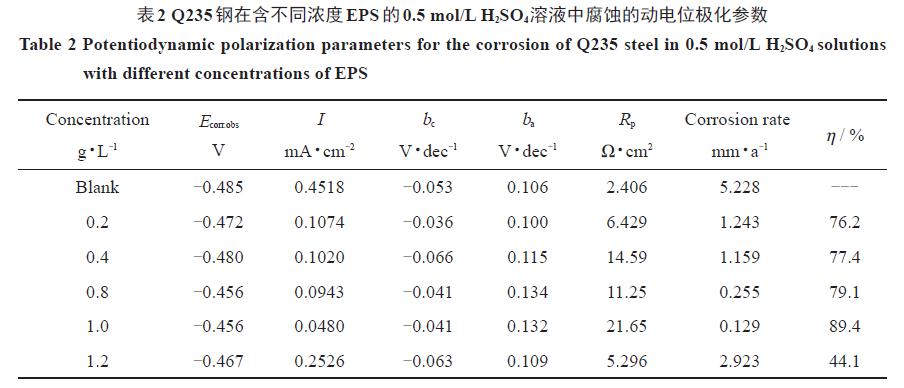
从图3 及表2 可以看出,当添加EPS后,Q235 钢在0.5 mol/L H2SO4 溶液中的极化电流密度逐渐减小,随着EPS 浓度的增加,极化电流密度随之减小,当EPS 浓度达到1.0 g/L 时,极化电流密度从空白溶液的0.4518 mA/cm2 减小到0.0480 mA/cm2。说明EPS 的加入,抑制了碳钢表面的腐蚀。此时缓蚀率达到最大,为89.4%。当继续增加EPS 浓度时,电流密度增大,缓蚀率降低。而极化电阻Rp随EPS 浓度的增加而增大,说明EPS 的加入抑制了表面电荷转移。这是因为EPS的吸附力较高,随EPS浓度增加,其在碳钢表面的覆盖逐渐致密。当EPS超过一定浓度时,缓蚀率降低,原因是其在碳钢表面的致密性遭到破坏。
3.3 表面形貌

图4 Q235 钢在含不同浓度EPS的0.5 mol/L H2SO4溶液中浸泡2 h 后表面形貌的SEM像
Fig.4 Surface morphologies of Q235 steel immersed in 0.5 mol/L H2SO4 solutions with 0 g/L (a), 0.8 g/L(b), 1.0 g/L (c) and 1.2 g/L (d) EPS for 2 h
图4a~d 分别为Q235 钢在未添加EPS,添加0.8,1.0 和1.2 g/L EPS 的0.5 mol/L H2SO4溶液中浸泡2 h后的表面SEM像。可以看出,未添加EPS 时,Q235钢表面腐蚀比较严重,可以较清晰的看到不同腐蚀区域边界。当添加0.8 g/L EPS时,其表面腐蚀减缓,虽可以看到一些腐蚀现象,但与未添加EPS 时的比较,表面更加平整。当EPS 浓度为1.0 g/L 时,可以看到Q235 钢表面较为光滑平整,基本看不到腐蚀,说明此时,能较好地控制H2SO4溶液对Q235 钢的腐蚀。当EPS 浓度超过1.0 g/L 时,可以看出表面出现了腐蚀现象,说明EPS 浓度超过1.0 g/L 时,EPS 对Q235 钢的缓蚀效率下降,表面膜层的致密性下降,这与电化学结果一致。
3.4 EPS成分测定
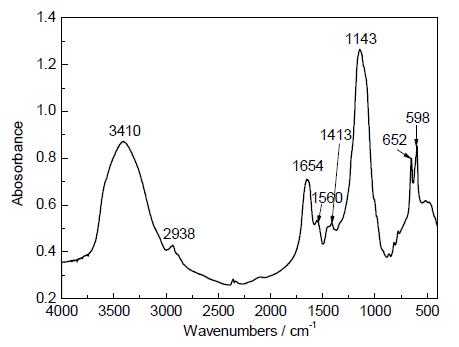
图5 EPS的Fourier红外吸收光谱
Fig.5 FT-IR spectrum of EPS
图5 为EPS的FT-IR 谱。通过图5 可以看出EPS的特征官能团。图5 中3400 cm-1 (3600~3200 cm-1)处的宽吸收峰为从弧菌培养液中提取出的EPS 的O—H伸缩峰[13,14];在2938 cm-1弱的吸收峰为脂肪族CH2基团中C—H伸缩振动峰,表明含有多糖或蛋白质[15];1654 cm-1 (1593~1662 cm-1) 为半乳糖或甘露糖中苯环的非对称伸缩振动峰[16];1560 cm-1为氨基化合物中C—N 的伸缩振动峰;1413 cm- 1 为—COOH的对称伸缩振动峰;1143 cm-1伸缩振动峰证明了多糖的存在[17];690~515 cm- 1 为伯胺中N—H 的振动峰。上述结果表明,EPS 含有较多的给电子基,如O—H,—COOH,N—H等。
3.5 吸附模型
缓蚀剂EPS与碳钢表面作用机理可以通过吸附等温线进行研究。EPS 分子量通过凝胶渗透色谱(GPC) 测定为29572 Da。EPS 与重金属之间的结合力较高,并且这种吸附符合Langmuir 吸附或Freundlich吸附[18,19]。通过比较,EPS在碳钢上的吸附较好地符合Langmuir吸附模型,则有下式:
C/θ=1/K+C (4)
式中,C 为EPS浓度;K 为吸附平衡常数。
对25 ℃时的C/θ 与C 进行线性拟合处理,结果如图6 所示。
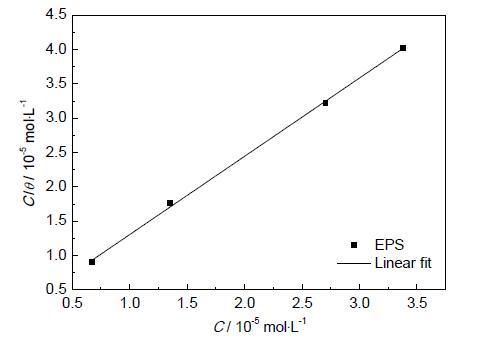
图6 Q235 钢在25 ℃时添加EPS的0.5 mol/L H2SO4溶液中的Langmuir吸附模型
Fig.6 Langmuir adsorption isotherm of EPS on Q235steel in 0.5 mol/L H2SO4 solutions at 25 ℃
可以看出,25 ℃时C/θ 与C 较好的符合线性关系。Gibbs 自由能ΔG0通过下式计算[20,21]:
K = (1/55.5)exp【-(ΔG0/RT)】 (5)
式中,R 为普适气体常数,取8.314 J/ (mol·K);T 为温度,取25 ℃。
通过计算得出25 ℃下Q235 钢在添加EPS 的0.5 mol/L H2SO4 溶液中的Gibbs 自由能ΔG 0 为-42.94 kJ/mol,相关线性系数为0.9987。根据At-kins[21]的研究结果,当|ΔG0|为20 kJ·mol-1或更小时,带电的分子与金属之间由静电相互作用吸附在金属表面,为物理吸附。当|ΔG0|达到约40 kJ·mol-1或者更大时,由于电子的转移或者共用形成共价键,为化学吸附。根据计算得出EPS 在Q235 钢表面的ΔG0为-42.94 kJ·mol- 1,为化学吸附;又ΔG0 小于零,故EPS在碳钢表面的吸附为自主吸附。
3.6 缓蚀机理
碳钢的腐蚀是从阳极氧化产生Fe2+开始的,反应如下:
Fe→Fe2+ +2e- (6)
而Fe2+在溶液中继续氧化生成Fe3+,而Fe3+会加速碳钢的腐蚀,它与碳钢表面的Fe发生如下反应:
Fe2+ →Fe3+ +e- (7)
Fe+2Fe3+ →3Fe2+ (8)
从上述反应中可以看出,固化Fe2+后就能控制碳钢的腐蚀。EPS主要是由多糖、核酸、蛋白质和腐蚀酸等组成,通过其FT-IR 可知,EPS 中含有O—H,—COOH和N—H等给电子基。Chongdar 等[22]的研究表明,EPS 通过给电子基团能与Fe2+或Fe3+结合,在碳钢表面形成一层Fe-EPS 保护层。Fe 与EPS 的结合力会影响Fe-EPS 层在碳钢表面的吸附强度及致密度。随着溶液中EPS浓度的增加,与Fe 能结合的EPS量增加,形成的Fe-EPS层在碳钢表面的致密度增加,从而增加对碳钢的保护力。Dong 等[23]研究了EPS 对Fe2+的结合力,发现随着EPS 浓度的增加,其对Fe2+的结合力增加。当EPS 达到一定浓度时,Fe2 +-EPS 层在碳钢表面较为致密。超过一定浓度后,Fe2+-EPS层在碳钢表面的吸附达到动态平衡,在表面无活性吸附点,会扰动吸附层。并且EPS 会结合溶液中的Fe3+,加速阳极Fe 的溶解,破坏保护层的致密性,从而降低了对碳钢的缓蚀作用。这就解释了本文中当EPS 浓度超过1.0 g/L 后,缓蚀率反而下降的原因,这点从SEM像也得到验证。
4 结论
(1) 胞外聚合物EPS 能有效抑制H2SO4 溶液对Q235 钢的腐蚀。EPS 对Q235 钢的最佳缓蚀浓度为1.0 g/L,此时缓蚀率为89.4%。
(2) EPS 中含有如羧基、氨基等带电子基团,这些基团能与Fe2+结合,形成Fe2+-EPS 层吸附在碳钢表面。
(3) EPS在Q235 钢表面的吸附符合Langmuir 吸附模型,且为自主的化学吸附。
参考文献
[1] Lozano I, Mazario E, Likhanova N V, et al. Corrosion behaviour ofAPI 5LX52 steel in HCl and H2SO4 media in the presence of 1,3-dibencilimidazolio acetate and 1,3- dibencilimidazolio dodecanoateionic liquids as inhibitors [J]. Mater. Chem. Phys., 2014, 147: 191
[2] Zhao J M, Li J. Corrosion inhibition performance of carbon steel inbrine solution containing H2S and CO2 by novel gemini surfactants[J]. Acta Phys.-Chim. Sin., 2012, 28(3): 623(赵景茂, 李俊。 新型双子表面活性剂在H2S 和CO2盐水溶液中对碳钢的缓蚀性能[J]. 物理化学学报, 2012, 28(3): 623)
[3] Banerjee S, Srivasrava V, Singh M M. Chemically modified naturalpolysaccharide as green corrosion inhibitor for mild steel in acidicmedium [J]. Corros. Sci., 2012, 59: 35
[4] Umoren S A, Ogbobe O, Igwe I O, et al. Inhibition of mild steel corrosionin acidic medium using synthetic and naturally occurringpolymers and synergistic halide additives [J]. Corros. Sci., 2008, 50:1998
[5] Lee W, Lewandowski Z, Nielsen P H, et al. Role of sulfate-reducingbacteria in corrosion of mild steel: A review [J]. Biofouling, 1995,8: 165
[6] Jin J T, Wu G X, Zhang Z H, et al. Effect of extracellular polymericsubstances on corrosion of cast iron in the reclaimed wastewater[J]. Bioresour. Technol., 2014, 165: 162
[7] Yildiz F H, Visick K L.Vibrio biofilms: so much the same yet so different[J]. Trends Microbiol., 2009, 17: 109
[8] Kavita K, Mishra A, Jha B. Isolation and physico-chemical characterisationof extracellular polymeric substances produced by the marinebacterium Vibrio parahaemolyticus [J]. Biofouling, 2011, 27(3): 309
[9] Cao C N, Zhang J Q. An Introduction to Electrochemical ImpedanceSpectroscopy [M]. Beijing: Science Press, 2002(曹楚南, 张鉴清。 电化学阻抗谱导论[M]. 北京: 科学出版社,2002)
[10] Farag AA, Hegazy M A. Synergistic inhibition effect of potassiumiodide and novel Schiff bases on X65 steel corrosion in 0.5 MH2SO4 [J]. Corros. Sci., 2013, 74: 168
[11] Guo W J, Chen S H, Huang B D, et al. Protection of self-assembledmonolayers formed from triethyl phosphate and mixed selfassembledmonolayers from triethyl phosphate and cetyltrimethylammonium bromide for copper against corrosion [J]. Electrochim.Acta, 2006, 52(1): 108
[12] Ganesh V, Pal S K, Kumar S, et al. Self- assembled monolayers(SAMs) of alkoxycyanobiphenyl thiols on gold—A study of electrontransfer reaction using cyclic voltammetry and electrochemicalimpedance spectroscopy [J]. J. Colloid Interface Sci., 2006,296:195
[13] Nwodo U U, Okoh A I. Characterization and fl occulation propertiesof biopolymeric fl occulant (glycosaminoglycan) produced byCellulomonas sp. Okoh [J]. J. Appl. Microbiol., 2013, 114: 1325
[14] Kavita K, Mishra A, Jha B. Extracellular polymeric substancesfrom two biofilm forming Vibrio species: Characterization and applications[J]. Carbohydr. Polym., 2013, 94: 882
[15] Iye A, Mody K, Jha B. Characterization of an exopolysaccharideproduced by a marine enterobacter cloacae [J]. Indian J. Exp. Biol.,2005, 43: 467
[16] Freitas, F, Alves V D, Pais J, et al. Characterization of an extracellularpolysaccharide produced by a Pseudomonas strain grown onglycerol [J]. Bioresour. Technol., 2009, 100: 859
[17] Cao B, Shi L, Brown R, et al. Extracellular polymeric substancesfrom Shewanella sp. HRCR-1 biofilms: Characterization by infraredspectroscopy and proteomics [J]. Environ. Microbiol., 2011,13: 1018
[18] Bhaskar P V, Bhosle N B. Bacterial extracellular polymeric substances(EPS): A carrier of heavy metals in the marine food-chain[J]. Environ. Int., 2006, 32: 191
[19] Moon S H, Park C S, Kim Y J, et al. Biosorption isotherms of Pb(II) and Zn (II) on Pestan, an extracellular polysaccharide, ofPestalotiopsis sp. KCTC 8637P [J]. Process Biochem., 2006, 41:312
[20] Zarrouk A, Hammouti B, Zarrok H, et al. N- containing organiccompound as an effective corrosion inhibitor for copper in 2MHNO3: Weight loss and quantum chemical study [J]. Der Pharm.Chem., 2011, 3(5): 263
[21] Atkins P W. Physical Chemistry [M]. 6th Ed. Oxford: Oxford UniversityPress, 1999
[22] Chongdar S, Gunasekaran G, Kumar P. Corrosion inhibition ofmild steel by aerobic biofilm [J]. Electrochim. Acta, 2005, 50:4655
[23] Dong Z H, Liu T, Liu H F. Influence of EPS isolated from thermophilicsulphate-reducing bacteria on carbon steel corrosion [J]. Biofouling,2011, 27(5): 487
责任编辑:王元
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





