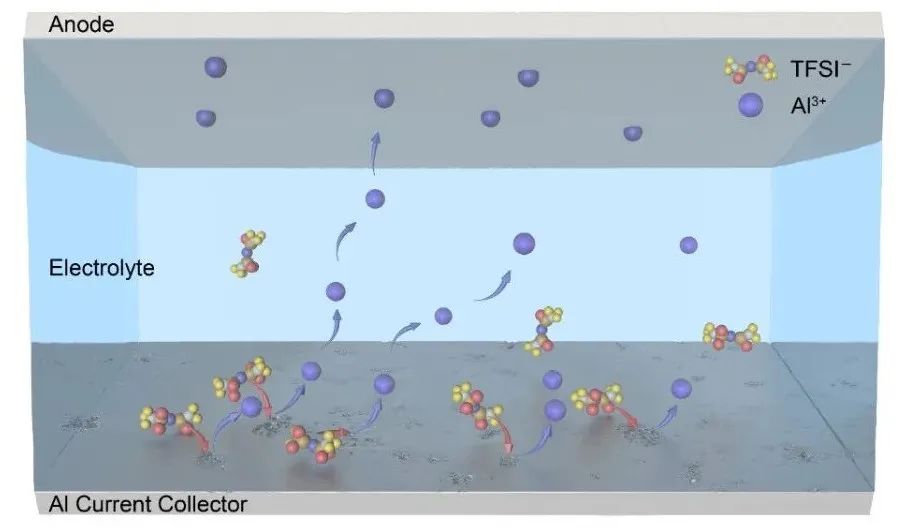
导读 铝箔是锂电池正极最常用的集流体,但其在高电压下的严重腐蚀问题不能满足可充电电池日益增长的能量密度需求。铝集流体腐蚀可能导致正极分层剥离、内阻增加、电解质分解等问题,从而导致电池过早失效。因此,系统地了解铝集流体腐蚀机理和有效的防腐蚀策略对于提升锂电池的整体性能是十分必要的。 研究背景 具有高能量密度和长循环寿命的锂离子电池(LIBs)已成为3C电子、电动汽车和智能电网的主要能源储能系统。然而,基于传统石墨(372 mAhg−1)负极LIBs的能量密度已接近其能量密度上限,这无法满足人们对能量密度日益增长的需求。对此,研究人员除使用具有超高理论容量(3860 mAhg−1)的锂金属负极外,还致力于提高电池工作电压(例如,>4.5 V vs. Li/Li+),通过使用层状氧化物Li[NixCoyMn1-x-y]O2或尖晶石LiNi0.5Mn1.5O4组成的高电压正极来进一步提高锂电池能量密度。 目前,研究人员主要关注高电压条件下,正极活性材料的失活和失效问题,然而,电池中的其他组成部分在高电压下的失效问题在很大程度上也决定着LIBs的整体性能。作为LIBs不可或缺的组成部分,铝(Al)因其高电子导电性、优异的化学稳定性、低密度和低成本等优势,是最常用的正极材料集流体。 然而,在高电压条件下,Al集流体腐蚀问题可能会导致活性材料与Al集流体的粘附力丧失,导致活性材料与Al集流体发生局部分层甚至分离,从而破坏正极和电池的结构稳定性。Al集流体腐蚀形成的副产物可能阻碍锂离子的传输,增加内阻,降低电子电导率,导致容量快速衰减和电池过早失效。 另外,在电池充放电过程中,Al集流体上形成的Al3+物质可能会溶解并沉积在负极表面,这可能会造成严重的电解质分解及锂枝晶生长,从而导致严重的电池故障和安全问题。因此了解高电压下Al集流体的腐蚀机制并解决这一问题,对于进一步提高锂电池的能量密度和整体性能意义重大。 锂电池中Al集流体的腐蚀机理 本工作重点关注了LiTFSI及LiFSI两种电解质的Al集流体腐蚀问题,LiTFSI基电解质对Al集流体的腐蚀主要是因为形成了较为稳定的Al(TFSI)3等含Al物种,其在电池循环过程中不断溶解,从而造成严重的Al集流体腐蚀问题(图1)。 图1 LiTFSI基电解质腐蚀Al集流体示意图 抑制Al腐蚀的策略 抑制Al集流体腐蚀的研究进展总结如图2所示,主要包括电解液(质)优化以及对Al集流体的修饰处理两个部分。
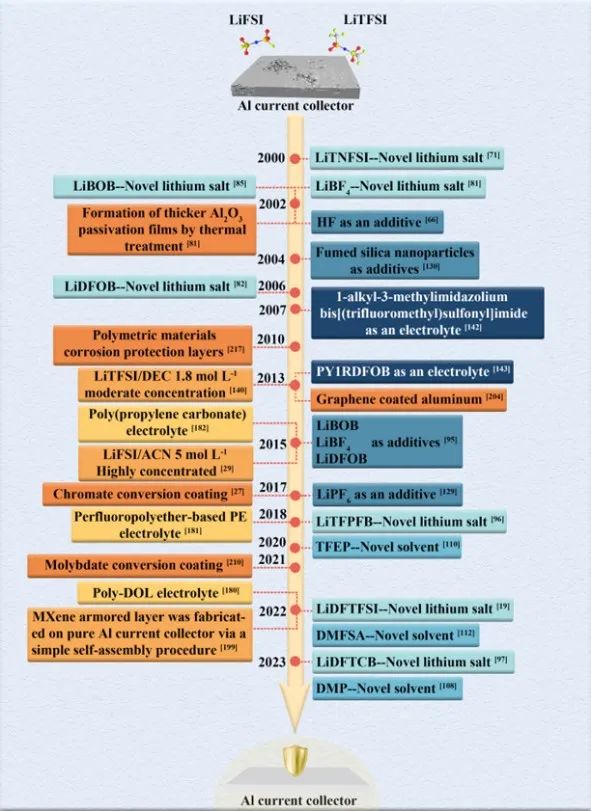
图2 抑制Al集流体腐蚀的研究进展
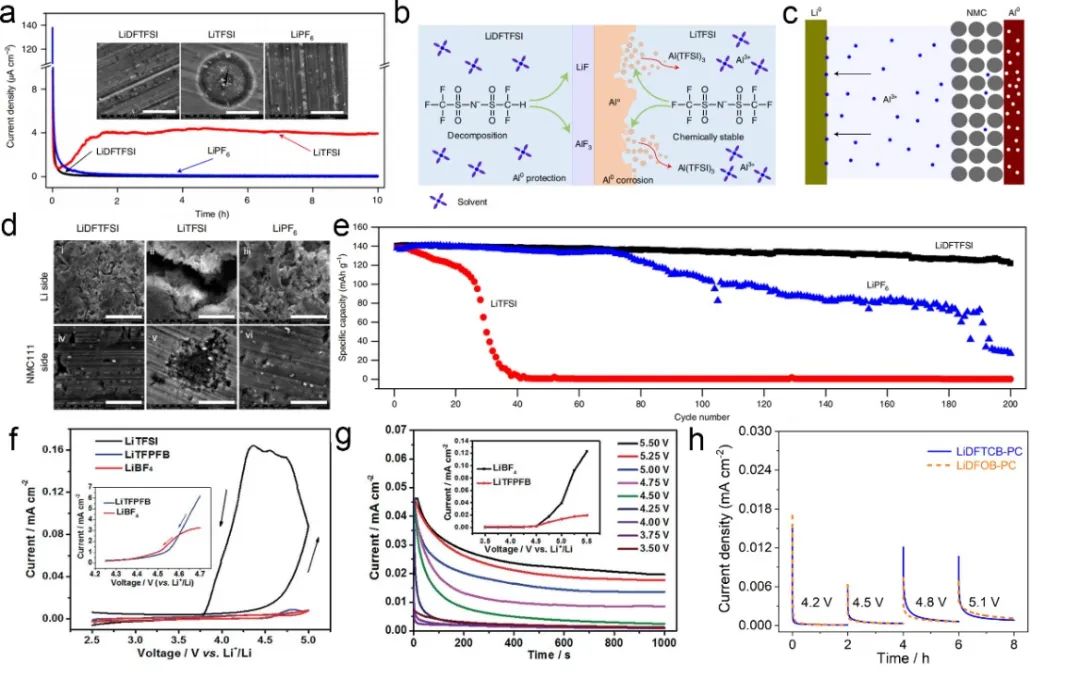
01 电解液(质)的优化 电解液(质)在决定锂电池的整体性能方面发挥着重要作用。根据上述腐蚀机制,调整锂盐、溶剂、电解液浓度以及使用其他类型的电解质,如离子液体和聚合物电解质,有利于抑制Al(TFSI)3的形成和溶解,从而防止Al集流体的严重腐蚀。 1 锂盐的优化 研究人员设计合成出多种新型锂盐,如Al中心、碳中心、硼中心、休克尔锂盐等,可以有效地钝化Al集流体,从而使其可以承受4.5 V以上的高电压。或利用多种锂盐之间的协同效应对Al集流体进行保护(图3)。 2 溶剂的优化 低介电常数的溶剂有利于抑制含Al物种的溶解,从而阻止Al集流体腐蚀。另外,溶剂分子在Al集流体表面分解形成保护层或者对溶剂进行氟化,降低含Al物种的溶解度可以有效减缓对Al集流体的腐蚀(图4)。
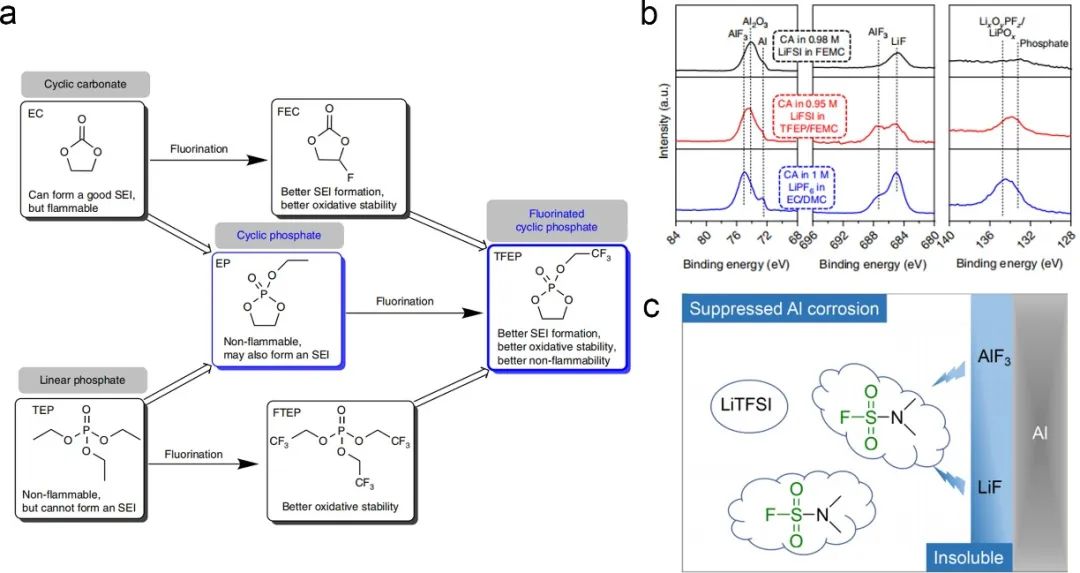
图4 (a)氟化环状磷酸酯溶剂的设计;(b)在三种不同电解液中完成CA测试后,Al箔的高分辨率XPS光谱;(c)DMFSA作为溶剂时抑制Al集流体腐蚀的机理示意图
3 抑制Al腐蚀的添加剂 少量添加剂的加入对于锂电池的性能提升具有很大帮助,常见的LiPF6、HF、硼盐等可以作为添加剂加入到电解液中,可以有效的钝化Al集流体,形成AlF3等保护层,抑制Al集流体腐蚀(图5)。
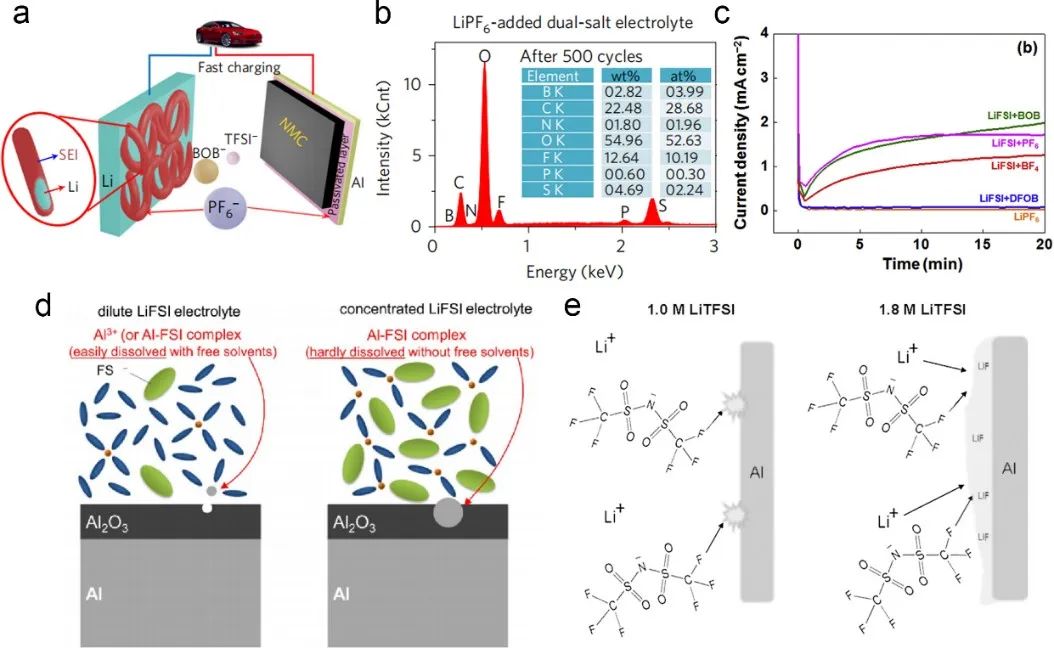
图5 (a)LiTFSI–LiBOB电解质中的LiPF6添加剂防止Al腐蚀并提高Li金属的稳定性示意图;(b)在含有0.05 M LiPF6添加剂的电解液循环后的Li金属负极的EDS能谱;(c)LiFSI+BF4、LiFSI+POB、LiFSI+DFOB、LiFSI+PF6和LiPF6中Al电极的CA曲线;(d)稀释LiFSI/AN电解液和高浓度LiFSI/AN-电解液示意图;(e)在1.0 M LiTFSI和1.8 M LiTFSI中LiTFSI分解和形成LiF界面膜的机制示意图
4 高浓电解液 5 离子液体电解质 6 聚合物电解质 聚合物电解质对含Al物种具有较差的溶解度,从而达到对Al腐蚀的抑制效果,另外还可以通过加入添加剂、提高锂盐浓度等手段来增强抑制效果(图6)。
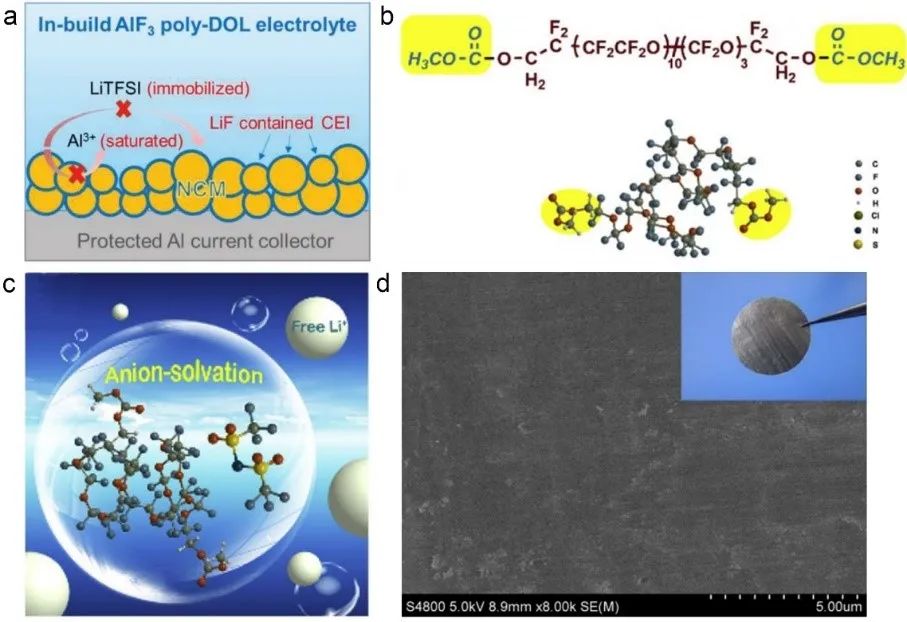
图6 (a)AlF3-Poly-DOL电解质中集流体腐蚀的示意图;(b)PFPE-MC的结构图;(c) 阴离子溶剂化相互作用的示意图;(d)LiFe0.2Mn0.8PO4||Li电池100次循环后Al集电极的SEM和照片(插图)
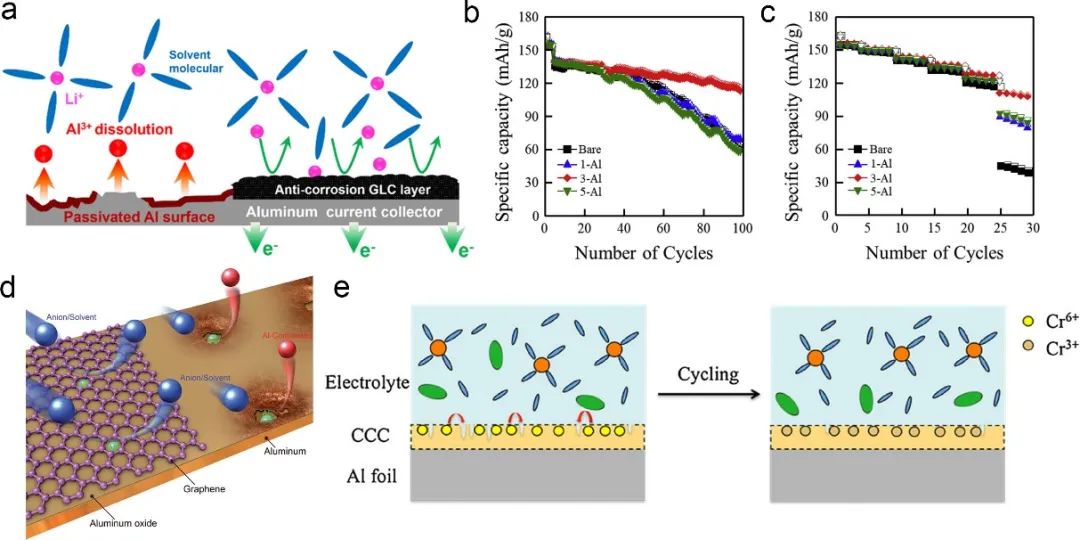
02 Al集流体的处理 预先对Al集流体进行表面处理也是防止Al腐蚀的有效策略之一。例如在Al表面涂覆碳材料(碳黑、石墨、石墨烯)涂层,可以有效的防止Al腐蚀并增大Al箔与正极材料间的接触面积,但同时也会牺牲能量密度。另外铬酸盐转换材料、Mxene和聚合物等也可以用作涂层来抑制Al集流体的腐蚀。 结论与观点 抑制Al集流体腐蚀对于提高锂电池能量密度至关重要,尽管已经在电解液的优化和Al集流体的处理方面付出了巨大的努力来提高Al集流体的稳定性,但从实际应用的角度来看,在提高电池的循环寿命、安全性和降低总成本方面仍有很大的发展空间。 因此,优化锂盐与溶剂,完善相关原位及非原位表征手段,结合实际应用开展相关测试是未来研究所需要重点关注的方向。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808414