摘 要:目的 研究P110S 低合金钢在H2S/CO2 环境中的腐蚀行为及腐蚀产物对其影响机理。方法 通过P110S 低合金钢在不同温度下的腐蚀失重实验、微观SEM 形貌观察、XRD 分析和离子选择性实验,探究腐蚀产物的晶体结构以及离子选择性对腐蚀行为的影响。腐蚀实验环境为模拟我国西北某油田现场不同井深的腐蚀工况,其中CO2 与H2S 的分压比为2.5。结果 温度低于100 ℃时,腐蚀产物主要为马基诺矿型FeS,其为阳离子选择性,能够阻碍阴离子与基体接触,起到抑制腐蚀的作用,因此腐蚀速率较低,约为0.15 mm/a,且随温度升高基本保持不变,试样表面的腐蚀产物膜平整未脱落;温度达到120 ℃后,腐蚀速率急剧增大,部分腐蚀产物由马基诺矿转变为磁黄铁矿,腐蚀产物膜因下层腐蚀产物挤压而发生破裂脱落,试样发生局部腐蚀;温度高于160 ℃时,腐蚀产物全部为磁黄铁矿型FeS,其为阴离子选择性,无法阻碍阴离子穿过腐蚀产物膜与基体接触,因此随着温度的升高,腐蚀速率逐渐增大并趋于平缓,达到3.6 mm/a。结论 H2S/CO2 环境中低合金钢腐蚀行为与腐蚀产物晶体构型及离子选择性密切相关,若腐蚀产物为马基诺矿型FeS 时,其具有阳离子选择性,能够抑制金属基体腐蚀溶解;而若腐蚀产物为磁黄铁矿型FeS 时,因其具有阴离子选择性,则不能抑制金属基体发生腐蚀溶解。
关键词:H2S/CO2 腐蚀;腐蚀产物;离子选择性;温度;低合金钢
含硫油气藏已经逐渐成为油气工业开采的主力,其中伴生的酸性气体H2S 不但会导致碳钢发生应力腐蚀开裂现象,还会使金属发生严重的腐蚀失重,甚至点蚀,直接威胁油气生产安全,因此H2S 腐蚀问题一直被研究者们所关注。
在腐蚀环境中,金属表面腐蚀产物的形成将直接影响腐蚀的进程[1-5]。碳钢在H2S 腐蚀环境下的腐蚀产物为硫化亚铁,由于温度、压力或者pH 值的不同,导致碳钢在不同环境下形成的硫化亚铁具有不同的晶体结构,例如四方薄片状马基诺矿(MackinawiteFeS)、立方硫铁矿(Cubic FeS)、单斜/六方磁黄铁矿(Pyrrhotite Fe1–xS)、六方陨铁矿(Troilite FeS)和正交黄铁矿(Pyrite FeS2)[6-7]。不同晶体结构的硫化亚铁构成的腐蚀产物膜对钢铁腐蚀行为的影响有明显区别[8],导致H2S 环境中的腐蚀机理更复杂,而H2S与CO2 共存时的腐蚀机理将更加复杂。孙乔[9]从离子选择性角度研究了腐蚀产物对低合金钢腐蚀速率的影响,发现低温时生成的陨铁矿为阳离子选择性,腐蚀速率较低且伴随着均匀腐蚀的发生;而高温下生成的马基诺矿为阴离子选择性,腐蚀速率较高,这说明腐蚀产物的离子选择性会影响腐蚀速率。Sato[10]提出了腐蚀产物具有离子选择性,从离子迁移角度对腐蚀产物影响腐蚀行为的机制进行讨论。后续的研究也表明,腐蚀产物的离子选择性是影响腐蚀行为的重要因素[11-12]。因此研究硫化亚铁晶体结构、离子选择性和腐蚀行为之间的关系,有助于进一步理解硫化氢对金属腐蚀的机制。
本文以油气田常用的P110S 低合金钢为研究对象,对其在H2S/CO2 环境下的腐蚀行为进行研究。通过高温高压腐蚀实验获得了P110S 在不同温度下的腐蚀速率、腐蚀形貌以及腐蚀产物组成,并结合点蚀坑截面结构和元素分布,以及腐蚀产物的离子选择性,对P110S 腐蚀行为随温度变化的机制进行讨论。
1 实验
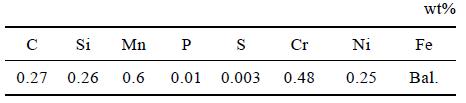
实验所用材料为油气田广泛应用的P110S 油管材料,其合金元素组成如表1 所示。
表1 P110S 的元素组成
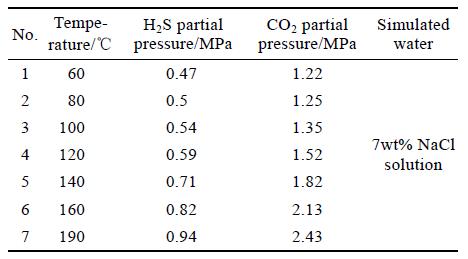
实验采用高温高压动态腐蚀试验方法,挂片尺寸(长×宽×厚)为50 mm×10 mm×3 mm。实验前,依次用120#、400#、800#砂纸打磨后,将试片浸没在丙酮中超声清洗并吹干,再用游标卡尺测量尺寸并用电子天平称量。实验时将试样挂载于动态高温高压反应釜中,实验周期为7 d。腐蚀实验环境为模拟我国西北某油田现场不同井深的腐蚀工况,工况参数见表2,其中CO2 与H2S 的分压比基本保持不变,为2.5。采用美国FEI 公司的场发射环境扫描电镜(Quanta200 FEG)对腐蚀后的试样进行形貌观察,采用BrukerD8 X-射线衍射仪对腐蚀产物组分进行分析。
表2 不同温度的腐蚀失重实验条件
腐蚀产物的膜电位测量是一种常用的表征腐蚀产物离子选择性的手段。首先,将试样上的腐蚀产物逐层刮取置入丙酮中,再使用超声波震荡使腐蚀产物分散均匀;然后,将腐蚀产物加入溶有醋酸纤维素的丙酮中,当丙酮全部自然挥发后,便可获得以醋酸纤维素为骨架的腐蚀产物膜。
根据Miyuki 的方法[13]进行膜电位测试,测试在室温(25 ℃)下进行。图1 为膜电位的测量装置示意图。如图所示,膜放置于两个容器的中间,左侧容器中的溶液依次为0.0001、0.001、0.01、0.1、1 mol/L氯化钾溶液,右侧容器中的溶液为0.01 mol/L 氯化钾溶液。当左右两侧容器中的氯化钾溶液浓度不同时,由于膜的离子选择性,在膜中迁移的阴阳离子数目将不同,此时膜的左右两侧会出现电势差,此电势差成为膜电位。使用两个饱和甘汞电极可以测量此电势差。
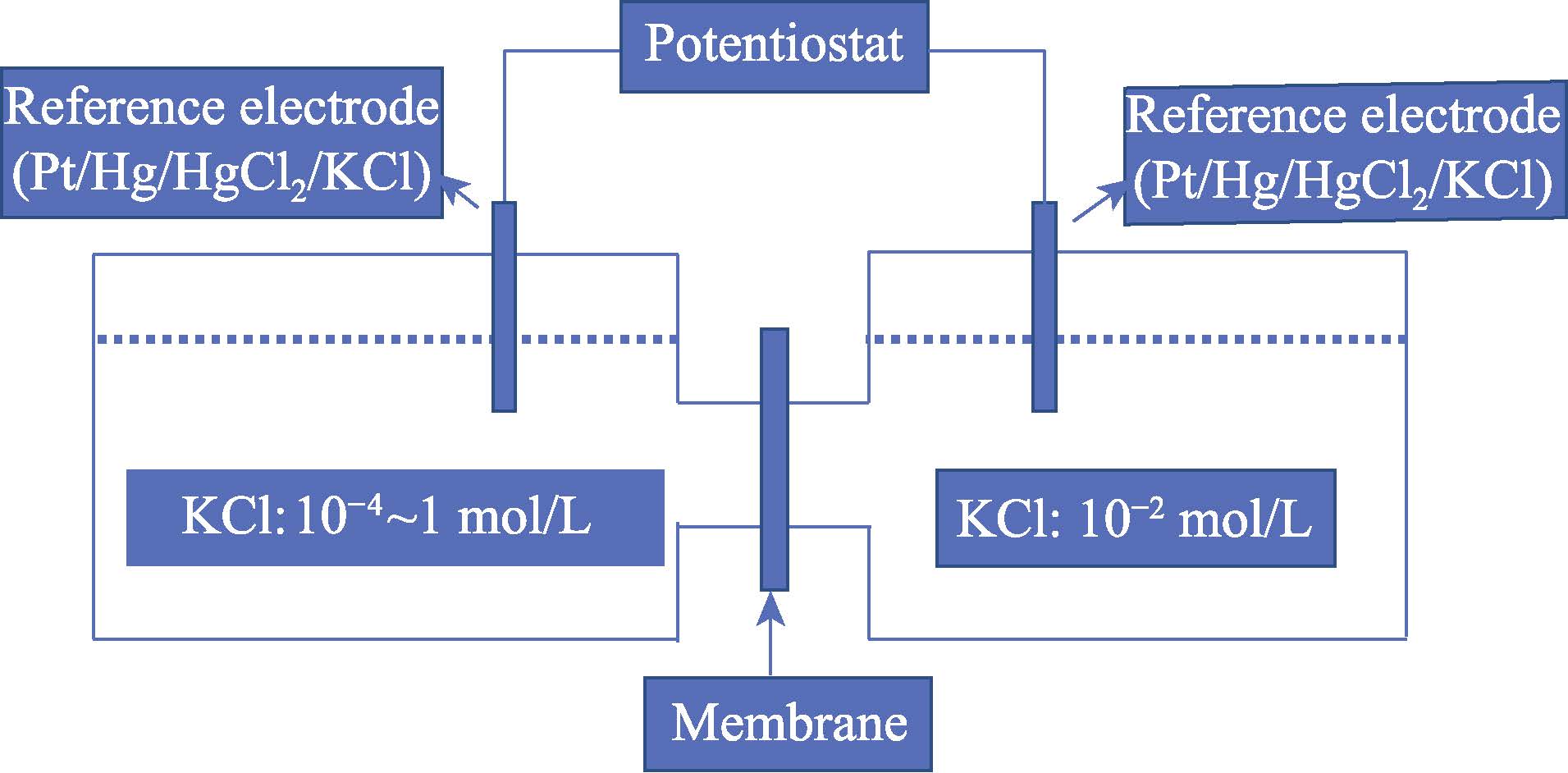
图1 膜电位的测量装置示意图
2 结果及分析
2.1 腐蚀速率
图2 为在不同温度H2S/CO2 腐蚀环境下低合金钢P110S 的腐蚀速率,总体来看,P110S 的腐蚀速率随着温度的升高而增加。以往的研究结果表明,CO2 腐蚀环境下,低合金钢的腐蚀速率会随着温度的升高,先上升后下降,其中腐蚀速率的最大值一般出现在60~ 80 ℃范围内[14-16]。而图2 中在60~190 ℃温度区间内,腐蚀速率持续增加,不符合CO2 腐蚀特征,因此在CO2 与H2S 分压比为2.5 的条件下,P110S 的腐蚀不由CO2 腐蚀控制。特别值得注意的是,当温度小于100 ℃时,P110S 的腐蚀速率几乎保持不变,腐蚀速率维持在0.15 mm/a 附近;而当温度进一步升高至120 ℃时,P110S 的腐蚀速率显著增加至 0.52mm/a,并且随着温度的升高,腐蚀速率继续快速增加,在190 ℃时高达3.61 mm/a。
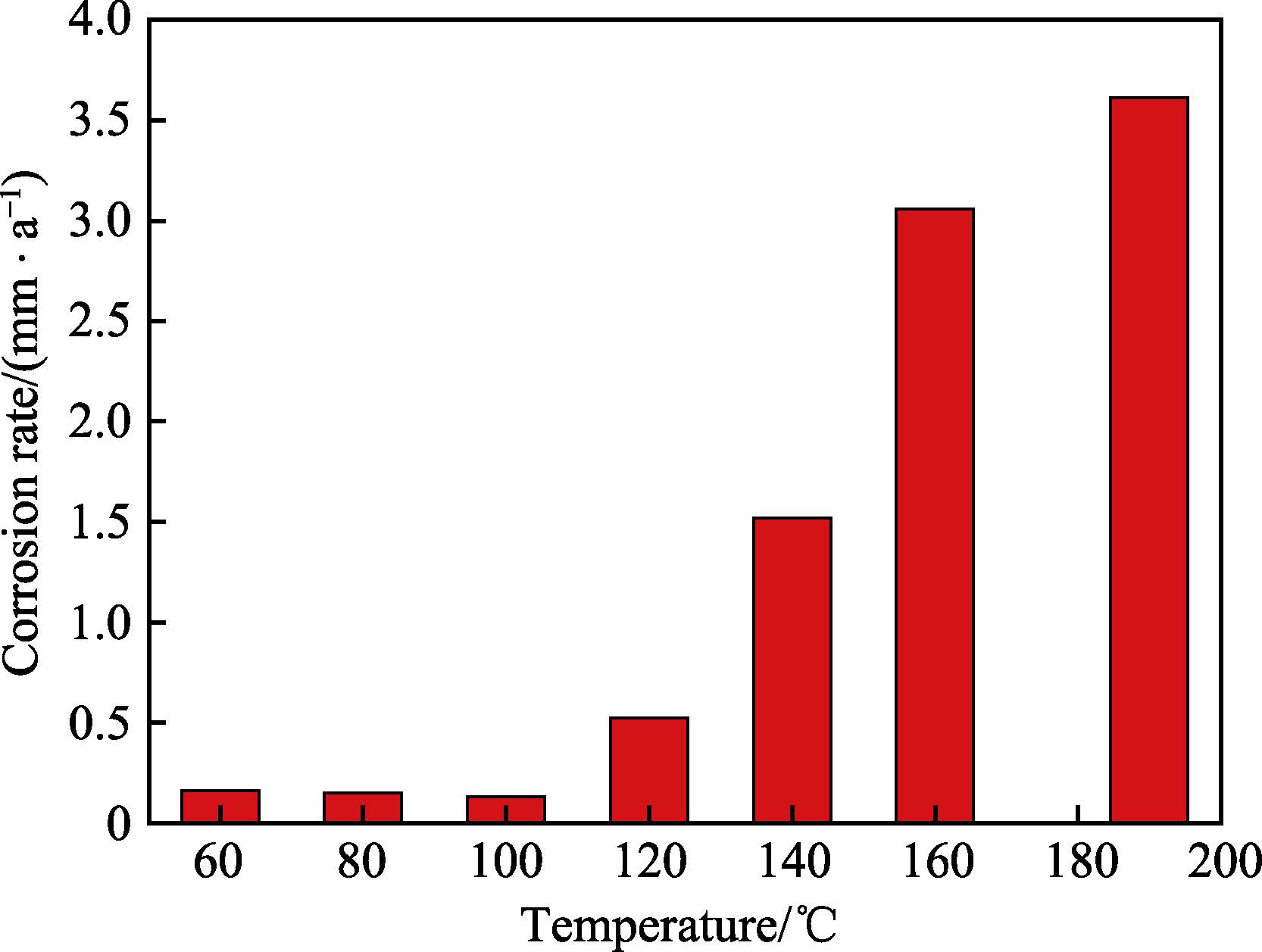
图2 不同温度条件下P110S 的腐蚀速率
2.2 宏观腐蚀形貌
图3 为P110S 在不同温度下的宏观腐蚀形貌。当温度低于100 ℃时,试样表面腐蚀较轻,整体上覆盖完整;当腐蚀温度升高至120 ℃时,试样表面的腐蚀产物膜出现鼓包现象,并且腐蚀产物膜形成的鼓包开始破裂,试样表面形成了局部腐蚀;当腐蚀温度升高至140 ℃时,腐蚀产物开始明显变厚且颜色变深,腐蚀产物膜导致的鼓包数量也开始有所增加;而当温度升高至160 ℃时,试样腐蚀进一步加剧,腐蚀产物膜形成的鼓包数量继续增多且分布均匀;当温度为190 ℃时,试样表面的鼓包现象最严重,鼓包尺寸比较大,腐蚀情况最严重。
2.3 微观腐蚀形貌
图4 为P110S 在不同温度下的腐蚀产物膜微观形貌。当温度为60 ℃和100 ℃时,试样表面的腐蚀产物平整,虽然在局部小区域内发生了轻微的脱落,但整体上覆盖完整;当腐蚀温度升至120 ℃时,试样表面的腐蚀产物膜出现鼓包,并且在鼓包状的腐蚀产物膜脱落处,金属基体发生明显的局部腐蚀;当腐蚀温度升高至140 ℃时,腐蚀产物开始明显增厚,鼓包状腐蚀产物膜的数量也开始显著增加,鼓包现象愈发严重;而当温度升高至160 ℃时,试样表面的腐蚀产物开始发生大面积的分层、脱落。值得注意的是,190 ℃时,试样表面每个鼓包状的腐蚀产物膜上出现了由晶体构成的同心环状结构。

图3 P110S 腐蚀后的宏观形貌

图4 不同温度下P110S 的微观腐蚀形貌(c 中右上角图片为鼓包状腐蚀产物破裂的形貌)
当温度为60 ℃和100 ℃时,试样表面形成的腐蚀产物未呈现出明显的晶体形状;而当腐蚀温度提高至140 ℃以上时,腐蚀产物呈现出规则的晶体形状,为六边片状结构,见图5a 所示。图5a、b 为形成在鼓包状的腐蚀产物膜内部的晶体形态,腐蚀产物由六边片状晶体交织而成,且每片晶体的厚度较薄,仅为36 nm。而在190 ℃,形成于鼓包状的腐蚀产物膜外的六边形晶体则发育较好,个体尺寸较大,厚度可大于1 μm。这种发育良好的六边形片状晶体仅形成在鼓包状的腐蚀产物膜的圆周上,并且呈现同心环状分布,应与鼓包状的腐蚀产物膜的生长有关。
2.4 腐蚀产物组成
图6 为P110S 在不同腐蚀温度下形成的腐蚀产物的XRD 图谱。实验结果表明,P110S 在CO2 与H2S分压比为2.5 的腐蚀环境中形成的腐蚀产物不含有FeCO3,均为铁的硫化物。当腐蚀温度小于100 ℃时,P110S 表面的腐蚀产物由马基诺矿组成,其中当温度为60 ℃时,腐蚀产物中还含有部分的立方硫铁矿,其可能是由马基诺矿转变而成;当腐蚀温度升高至120 ℃时,腐蚀产物中开始出现磁黄铁矿,并且随着温度的进一步升高,磁黄铁矿的含量不断增加;当温度达到190 ℃时,腐蚀产物完全由磁黄铁矿组成。因此马基诺矿向磁黄铁矿转变的温度为120 ℃,完全转变温度为190 ℃。结合前文的试验结果,腐蚀速率、腐蚀产物形貌随温度转变的规律相一致,因此P110S 的腐蚀过程受试样表面形成腐蚀产物类型的控制。

图5 不同温度条件下P110S 腐蚀形貌的微观SEM 形貌
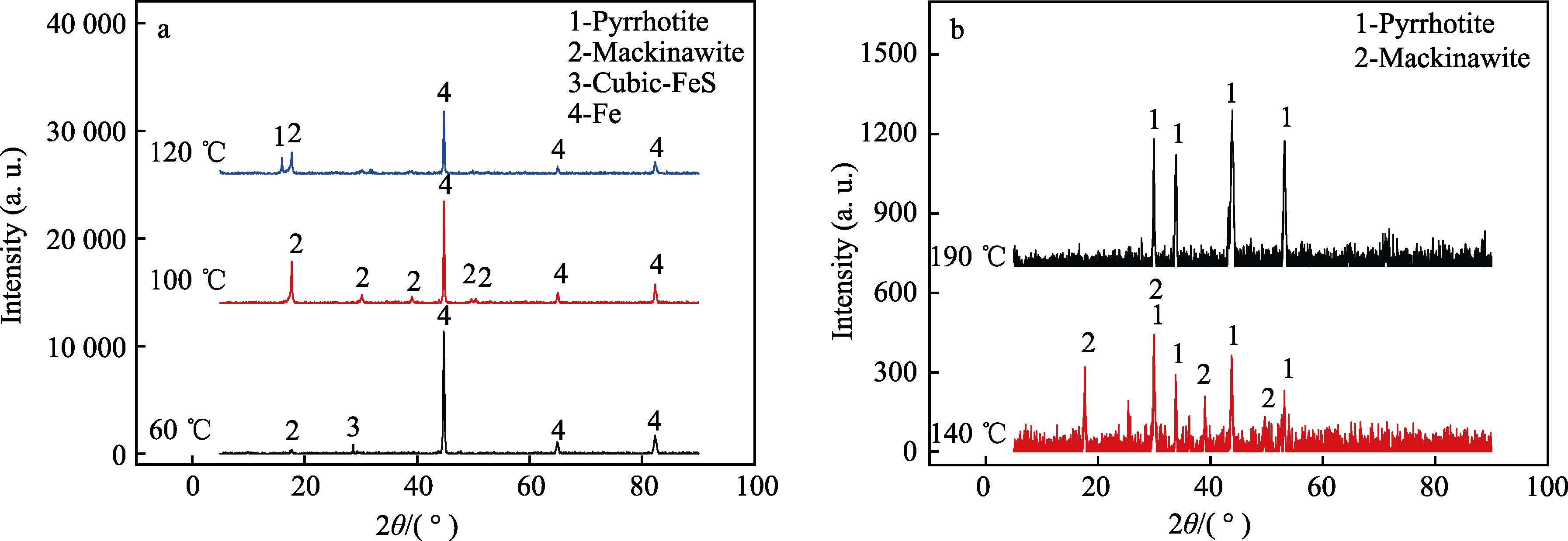
图6 不同温度下P110S 腐蚀产物的XRD 图谱
2.5 腐蚀产物截面
图7 为190 ℃腐蚀环境下腐蚀产物膜形成鼓包的截面形貌以及腐蚀产物的元素分布。结果表明,在鼓包的下方金属基体形成点蚀,并且在点蚀坑底部存在无腐蚀产物填充的空腔。蚀坑内的腐蚀产物由Fe、S、O 和Cl 元素组成,其中O 元素的含量较少。根据点蚀坑内元素的分布,可以发现坑内腐蚀产物分为两层:上层是由Fe 和S 元素组成的磁黄铁矿层,其分布区域见图7 中S 元素分布范围;而下层则主要由Fe、Cl 和O 元素组成,其分布区域见图7 中Cl 和O元素的分布范围。Cl 元素主要分布在点蚀坑底部,且含量明显增高,这是点蚀生长自催化酸化机制的重要特征[17-18],同时点蚀坑底部也有空腔形成,这都表明腐蚀产物膜导致的鼓包下的点蚀坑内一直处在快速酸性活化溶解状态。
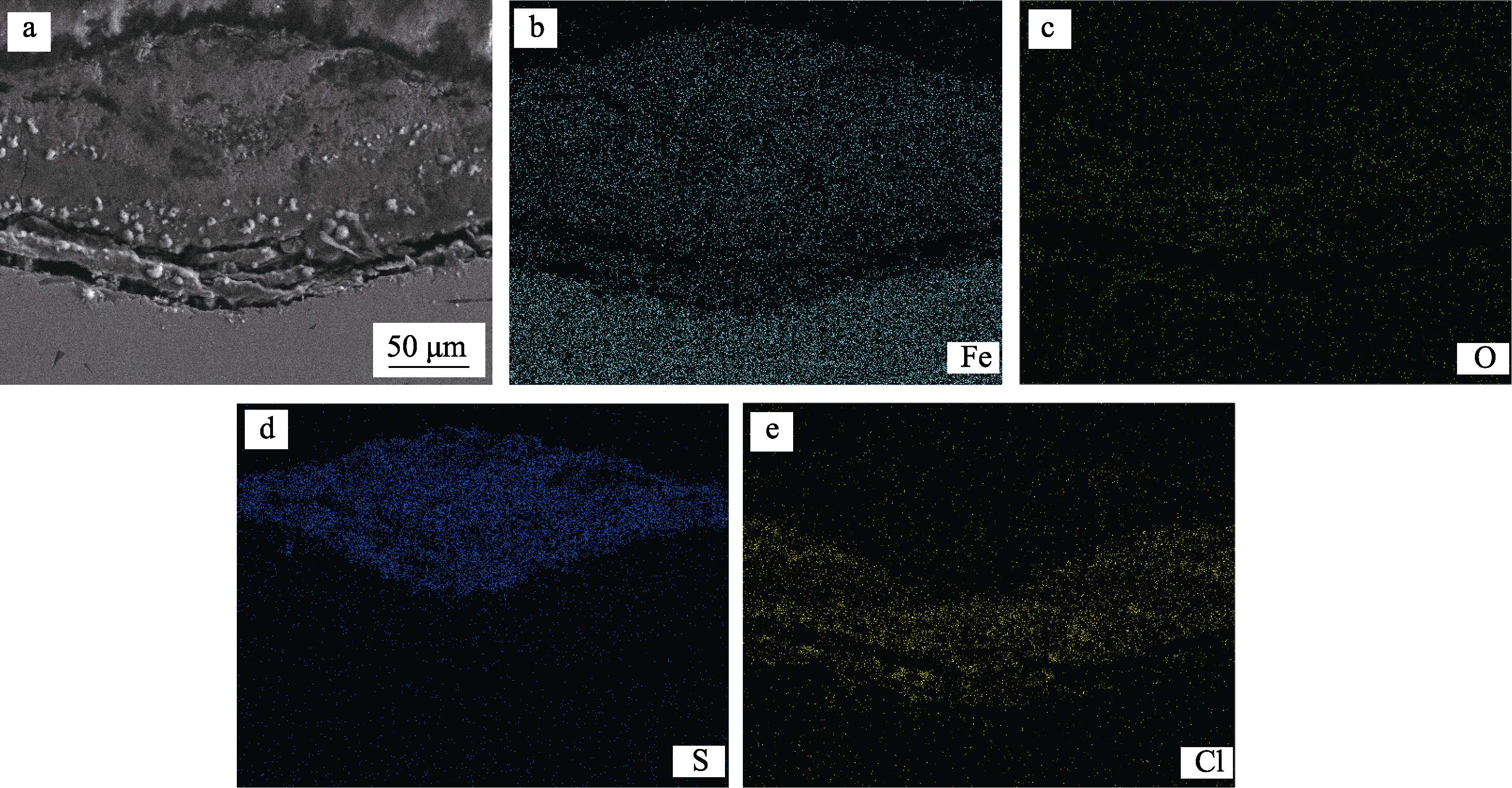
图7 190 ℃鼓包状腐蚀产物的截面形貌及元素分布
2.6 腐蚀产物离子选择性
腐蚀产物通常具有离子选择性,将影响溶液和基体金属表面之间的离子传输,进而影响金属基体的腐蚀过程。膜电位试验是表征腐蚀产物离子选择性最常用的实验方法。图8 为60、100、120、160 ℃下腐蚀产物的膜电位随KCl 浓度变化的曲线,结果表明,形成于60 ℃和100 ℃的腐蚀产物的曲线斜率为负,而形成于120 ℃和160 ℃的腐蚀产物的曲线斜率为正。曲线斜率为正表示腐蚀产物具有阴离子选择性,而曲线斜率为负表示腐蚀产物具有阳离子选择性。值得注意的是,腐蚀速率在100 ℃和120 ℃之间出现了拐点,而与之同时腐蚀产物的离子选择性也发生了转变,由马基诺矿转变为磁黄铁矿膜电位的结果表明。膜电位和XRD 的实验结果表明,形成于较低温度的马基诺矿具有阳离子选择性,而形成于较高温度的磁黄铁矿具有阴离子选择性。
图8 不同温度下腐蚀产物膜的离子选择性
3 讨论
腐蚀环境中CO2 与H2S 分压之比为2.5 时,不同于CO2 腐蚀,P110S 的腐蚀速率始终随着温度的升高而增加(图2),且在各温度下形成的腐蚀产物都为铁的硫化物,不含有FeCO3(图6),表明腐蚀过程一直受H2S 腐蚀控制。当腐蚀温度为120 ℃时,P110S的腐蚀速率、腐蚀形态以及腐蚀产物的组成都发生了明显的改变;当温度低于120 ℃时,腐蚀产物为单一的马基诺矿;而当温度高于120 ℃时,腐蚀产物则向磁黄铁矿转变;当温度到达190 ℃时,腐蚀产物中不再含有马基诺矿,完全由磁黄铁矿组成。腐蚀产物为马基诺矿时具有阳离子选择性,能够阻止溶液中的阴离子进入到腐蚀产物内。而腐蚀产物中有磁黄铁矿生成时,腐蚀产物的离子选择性会转变为阴离子选择性,使得阴离子能够穿过腐蚀产物到达金属基体表面,并在此处聚集。高浓度的Cl–造成严重局部酸化,导致金属基体处于活化溶解状态,从而导致点蚀的形成。因此,腐蚀产物离子选择性的转变是P110S在高温环境腐蚀速率快速增加和发生点蚀的主要原因。
腐蚀产物的离子选择性不但影响着P110S 的腐蚀速率,还直接影响着腐蚀产物的形貌。当腐蚀温度小于120 ℃时,阳离子选择性的腐蚀产物会阻止阴离子迁移,因此只能由Fe2+从金属基体表面迁移穿过腐蚀产物层,与溶液中的阴离子结合形成新的腐蚀产物,此时腐蚀产物的生长方向指向溶液,为向外生长。新的腐蚀产物在原有腐蚀产物上逐层生长,最终在试样表面形成平整的腐蚀产物层。而当温度高于120 ℃时,阴离子选择性的腐蚀产物阻挡了Fe2+迁移,此时只能由阴离子迁移穿过腐蚀产物,在金属基体和腐蚀产物的界面处形成新的腐蚀产物层,此时腐蚀产物的生长方向指向金属基体,为向内生长。一旦Cl–在局部聚集造成酸化,金属加速溶解,腐蚀产物就会快速增厚,导致鼓包状腐蚀产物的形成,并且底层腐蚀产物快速增加会导致上层腐蚀产物开裂。腐蚀产物一旦开裂,之前被限制在腐蚀产物下的Fe2+会迁移到开裂处,与溶液中S2–结合形成磁黄铁矿。由于此时阴、阳离子迁移都不再受到阻碍,生成的磁黄铁矿能够快速生长,形成的晶粒尺寸较大,如图4f 和图5c 所示。但是当磁黄铁矿生长到一定程度时,就会封堵腐蚀产物的裂口,使腐蚀产物回到向内生长的模式,直到下一次腐蚀产物层破裂。随着腐蚀产物不断开裂,就会在鼓包处形成同心的磁黄铁矿晶体环(如图4f 所示)。
4 结论
1)当温度在100 ℃以下时,随着温度的升高,P110S 低合金钢的腐蚀速率基本不变;温度在120 ℃至160 ℃之间时,随着温度的升高,腐蚀速率急剧上升,在160 ℃时达到3 mm/a;继续升高温度,腐蚀速率缓慢上升并保持在一个较高水平。
2)腐蚀产物的晶体构型和腐蚀产物膜形貌与温度密切相关。温度低于100 ℃时,腐蚀产物为马基诺矿,腐蚀产物膜平整致密,无脱落现象。温度上升至120 ℃时,腐蚀产物部分由马基诺矿转变为磁黄铁矿,腐蚀产物膜局部区域发生鼓包脱落,基体发生局部腐蚀,随着温度的升高,腐蚀产物中磁黄铁矿含量增加,腐蚀产物膜鼓包脱落愈发严重。当温度升高至190 ℃时,腐蚀产物全部为磁黄铁矿。
3)马基诺矿为阳离子选择性,能够阻止溶液中阴离子穿过其组成的腐蚀产物膜,因此当温度低于100 ℃时,腐蚀速率较低。而磁黄铁矿为阴离子选择性,溶液中的阴离子能够轻易穿过其构成的腐蚀产物膜,并与金属基体接触,使金属发生腐蚀溶解,因此当温度升高至120 ℃后,P110S 的腐蚀速率随温度升高而增大,当温度升高至190 ℃时,腐蚀产物已全部转变为磁黄铁矿,因此其腐蚀速率保持在高水平。
参考文献:
[1] SMITH J S, MILLER J D. Nature of sulphides and theircorrosive effect on ferrous metals: A review[J]. Britishcorrosion journal, 1975, 10(3): 136-143.
[2] BAI Peng-peng, ZHAO Hui, ZHENG Shu-qi, et al. Initiationand developmental stages of steel corrosion in wetH2S environments[J]. Corrosion science, 2015, 93: 109-119.
[3] ZIMER A M, DE CARRA M A, RIOS E C, et al. Initialstages of corrosion pits on AISI 1040 steel in sulfidesolution analyzed by temporal series micrographs coupledwith electrochemical techniques[J]. Corrosion science,2013, 76: 27-34.
[4] TANG Jun-wen, SHAO Ya-wei, GUO Jin-biao, et al. Theeffect of H2S concentration on the corrosion behavior ofcarbon steel at 90 ℃[J]. Corrosion science, 2010, 52(6):2050-2058.
[5] MORSE J W, MILLERO F J, CORNWELL J C, et al. Thechemistry of the hydrogen sulfide and iron sulfide systems innatural waters[J]. Earth-science reviews, 1987, 24(1): 1-42.
[6] RICKARD D, LUTHER G W. Chemistry of iron sulfides[J].Chemical reviews, 2007, 107(2): 514-562.
[7] WEN Xiang-li, BAI Peng-peng, LUO Bing-wei, et al. Reviewof recent progress in the study of corrosion products ofsteels in a hydrogen sulphide environment[J]. Corrosionscience, 2018, 139: 124-140.
[8] 范亚萍, 周怡诺. 不同温度下H2S/CO2 腐蚀产物膜对T95 套管腐蚀行为的影响[J]. 表面技术, 2016, 45(10):180-186.FAN Ya-ping, ZHOU Yi-nuo. Effects of H2S/CO2 corrosionscale on corrosion behavior of T95 casing steel at differenttemperature[J]. Surface technology, 2016, 45(10): 180-186.
[9] SUN Q, CHEN C F, ZHAO X, et al. Ion-selectivity ofiron sulfides and their effect on H2S corrosion[J]. Corrosionscience, 2019, 158: 108085.
[10] SATO N. Toward a more fundamental understanding ofcorrosion processes[J]. Corrosion science, 1989, 45(5):354-368.
[11] HUANG F, CHENG P, ZHAO X Y, et al. Effect of sulfidefilms formed on X65 steel surface on hydrogen permeationin H2S environments[J]. International journal of hydrogenenergy, 2017, 42(7): 4561-4570.
[12] TOMIO A, SAGARA M, DOI T, et al. Role of alloyedmolybdenumon corrosion resistance of austenitic Ni-Cr-Mo-Fe alloys in H2S-Cl− environments[J]. Corrosion science,2015, 98: 391-398.
[13] MIYUKI H, YAMASHITA M, FUJIWARA M, et al. Ionselective properties of rust membranes and protective effectof stable rust layer formed on weathering steel[J]. Zairyoto-kankyo,1998, 47(3): 186-192.
[14] 常炜, 胡丽华. 温度对X65 和3%Cr 管线钢CO2 腐蚀行为的影响[J]. 腐蚀与防护, 2012, 33(S2): 100-105.CHANG Wei, HU Li-hua. Effect of temperature on CO2corrosion behavior of X65 and 3%Cr pipeline steels[J].Corrosion and protection, 2012, 33(S2): 100-105.
[15] 杨建炜, 章军, 曹建平, 等. 温度对管线钢H2S/CO2 腐蚀行为的影响[J]. 材料工程, 2011(1): 87-91.YANG Jian-jun, ZHANG Jun, CAO Jian-ping, et al. Effectof temperature on H2S/CO2 corrosion behavior of pipelinesteel[J]. Materials engineering, 2011(1): 87-91.
[16] 李国敏, 刘烈伟, 郑家燊. 碳钢在含硫化氢及高压二氧化碳饱和的NaCl 溶液中的腐蚀行为[J]. 中国腐蚀与防护学报, 2000(4): 204-210.LI Guo-min, LIU Lie-wei, ZHENG Jia-shen. Corrosionbehavior of carbon steel in high pressure carbon dioxidesaturated NaCl solutions containing hydrogen sulfide[J].Journal of Chinese society for corrosion and protection,2000(4): 204-210.
[17] WANG Xin, XU Jin, SUN Cheng. Effects of sulfatereducingbacterial on corrosion of 403 stainless steel insoils containing chloride ions[J]. International journal ofelectrochemical science, 2013, 8(1): 821-830.
[18] THURMAN R B, GERBA C P, BITTON G. The molecularmechanisms of copper and silver ion disinfection ofbacteria and viruses[J]. Critical reviews in environmentalcontrol, 1989, 18(4): 295-315.
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。
-
标签: H2S/CO2 腐蚀, 腐蚀产物, 离子选择性, 温度, 低合金钢

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808414






