摘要
海洋油气管道作为大量、长距离输送油气资源最主要的方式,担负着海上油气集输的重要任务,也被称为海洋油气工程的“生命线”。然而海洋环境下的微生物腐蚀是造成海洋油气管道腐蚀损伤的重要原因之一。本文结合海洋油气输送管道的服役环境,综述了海洋环境下临海管道微生物腐蚀失效的研究进展,重点介绍了有代表性的硫酸盐还原菌和铁氧化菌在海洋环境下引起的微生物腐蚀规律和机理,并在此基础上总结了相应的海洋管道防护方法,为微生物腐蚀损伤的研究及控制提供参考。
关键词: 临海管道 ; 微生物腐蚀 ; 腐蚀防护
海洋中的管线,比起陆地环境中的而言,腐蚀更为严重,而且不易维修。海洋管道腐蚀不仅仅造成材料的浪费、环境的污染,更严重地是因腐蚀造成的油、气泄露引发灾难性事故。据统计,在海底管道发生失效的事故中,腐蚀引起的事故约占50%的比例,每年因腐蚀带来的经济损失约占各个国家国民生产总值的2%~4%。因此,在海洋石油开发领域,海洋腐蚀问题给人类带来了巨大的困扰,海上石油开发过程中的管道腐蚀与防护问题亟待解决[1]。
由于海洋环境复杂,对于海洋管道钢铁材料而言,除了受到海水的化学腐蚀、电化学腐蚀,还受到海洋微生物、生物的附着和污损[2-4]。海水环境中微生物腐蚀 (MIC) 最为普遍,与其相关的腐蚀失效和破坏已达到涉海材料总量的20%[5]。目前海洋环境已发现众多微生物菌群,包括古菌、病毒、酵母菌、放线菌、真菌以及与腐蚀相关的各种细菌[6],约占全球微生物数量的13%。研究表明微生物的菌落结构及活性均会随着海水的深度的变化而变化,如临海区、浅海区等氧气含量丰富的位置,藻类[7]、海洋生物、铁氧化细菌、霉菌等引起的海洋污损严重,而在海泥区,以硫酸盐还原菌 (SRB) 为主的厌氧微生物会引发腐蚀过程的发生。在我国辽东湾以及南海珠江口东部海底沉积物中SRB含量高达460、913个/克湿泥。在海洋底泥中,尤其是在低溶解氧条件下,高含量的SRB明显加速金属材料的腐蚀速度。
我国的海洋输送管线材料主要包括两类:金属材料和非金属材料,其中海洋油气管线主要以金属管道为主。根据实际应用条件的不同,金属管线材料分为碳钢管道、不锈钢管和铜镍合金管等。碳钢管线材料由于其成本低廉,力学性能优良从而在我国被广泛应用,碳钢管道中X65、X70、X80管线钢是油气管道常用的材料。此外,X100和X120等新型超高强度的管线钢也在工程中逐步应用[8]。不锈钢虽然具有良好的耐蚀性能,但海水中的点蚀穿孔现象以及高昂的成本往往限制了部分不锈钢的应用。铜及铜镍合金管道被普遍认为是兼具了耐海水腐蚀和耐海洋生物腐蚀的优良性能。然而一些研究却表明铜及其合金材料并不能有效防止SRB引起的腐蚀[9],铜在SRB存在的条件下反而会遭受严重的微生物腐蚀。因此,对于实际应用中的海洋油气输送管线受到的海洋微生物腐蚀尤其是SRB造成的腐蚀研究非常重要。
因此,为保证管道的安全运作,研究海水环境中管道的腐蚀特征、实时检测管道腐蚀状态,己成为亟待解决的焦点问题[10,11]。鉴于海洋管线腐蚀的危害性与海洋环境的复杂性,研究海洋钢铁材料的微生物腐蚀机制具有重要意义。近年来,人们从微观和宏观两个角度,对微生物腐蚀特征、机制等做了大量的研究。此工作旨在系统总结临海管道腐蚀特征与机制,重点讨论临海环境微生物腐蚀机制,总结目前海洋腐蚀与防护研究所面临的挑战,并对未来的发展方向进行展望,为更好地认识微生物污损行为和开发环保型方法提供理论支撑。
1 临海环境海洋腐蚀特征及微生物腐蚀规律
一般说来,临海环境海洋腐蚀主要集中在以下几方面:(1) 海洋大气环境腐蚀。该腐蚀环境为高盐含量、高湿度的大气环境,且氧气供应充分,但该区域微生物腐蚀的影响较少。(2) 海水飞溅干湿交替的环境腐蚀。在高潮线以上的海水飞溅区受波浪与潮汐作用,海水飞溅携带的腐蚀性离子在干热交替环境下易对钢结构造成较强的腐蚀作用。此区域供氧充分,导致腐蚀加剧,腐蚀率远远高于全浸区或海洋大气区。(3) 海洋潮差区腐蚀。海洋潮差区的腐蚀与海水的飞溅区不同,虽然潮差区也属于干湿交替的腐蚀环境,但由于潮水的涨落使得潮差区的干湿交替具有稳定的周期。这种周期性的干湿交替也会使得海水中某些好氧微生物周期性的附着在金属表面。(4) 全浸区腐蚀。海洋全浸区是指海水最低潮位下0.2~2 m的区域,也是微生物腐蚀最活跃的区域之一。材料在此区域不仅受到海水溶解氧、盐度、温度、流速、pH等各类环境因素的腐蚀影响,海水中大量的好氧菌如铁氧化细菌、铜绿假单胞菌等也会对该区域金属设备造成极大腐蚀破坏,微生物污损作用不容忽视[12]。(5) 海泥区腐蚀。海泥区一般被认为是海洋环境中腐蚀情况较轻微的区域,然而由于其低含氧量和富营养成分,海泥区为厌氧菌如硫酸盐还原菌等提供了良好的生存环境。在底泥表层 (底泥和海水界面) 处由于厌氧微生物作用导致的微生物腐蚀会加速附近位置基体管线材料腐蚀失效。特别是海陆交汇环境,海水和淡水交界位置,是厌氧微生物硫酸盐还原菌生长繁殖旺盛的位置,微生物腐蚀是关键失效原因之一[13-15]。
2 海洋管线腐蚀类型及腐蚀机制
海底管道输送的介质主要有原油、天然气、地层水及其混合物,海底管线主要腐蚀类型大体分为内腐蚀和外腐蚀两种。内腐蚀的主要包括CO2/H2S酸性气体腐蚀、垢下腐蚀、微生物腐蚀等;外腐蚀主要来源于海底管道所处的海水环境,主要有海水腐蚀和海底底泥腐蚀。海底管线内外受到各种形式的腐蚀破坏,本文将概述常见典型的微生物腐蚀、缝隙腐蚀、应力腐蚀开裂,及多种腐蚀现象并存并相互促进的腐蚀失效模式。
2.1 微生物腐蚀
海洋环境中与腐蚀相关的微生物主要包括细菌、真菌及藻类,尤其以细菌为主。腐蚀性细菌又分为好氧菌和厌氧菌,前者主要包括铁代谢菌 (IOB),后者主要指SRB[16]。海洋环境中SRB、IOB是普遍存在的,研究其造成的金属腐蚀具有典型性,可以得到许多具有普适性的观点和结论。而目前的研究表明,SRB在缺氧环境中,是最具有腐蚀性的关键微生物种类之一[17]。IOB好氧细菌主要活跃在富氧的海水区,除了其自身对基体材料造成的腐蚀,通常和SRB具有协同作用,加速金属的腐蚀。
2.1.1 硫酸盐还原菌的腐蚀机理
常压下在海水区与底泥区有关SRB对金属的腐蚀机理主要包括以下3种:
(1) 阴极去极化理论。该理论认为金属作为阳极失去电子被腐蚀,介质中的质子得到电子在金属表面产生H,SRB在氢化酶作用下消耗H,从而在腐蚀过程中促进阴极去极化的作用,加速腐蚀。涉及如下反应:
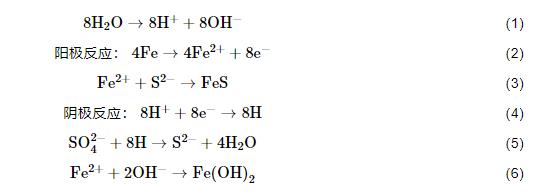
总反应:
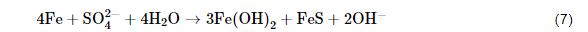
(2) 代谢产物去极化理论。传统的腐蚀理论认为微生物并未直接参与到金属腐蚀过程中,而是微生物的代谢产物对金属产生腐蚀作用。SRB腐蚀的发生与生物膜密不可分,生物膜在金属材料表面吸附和生长在非常短时间内就可以完成,生物膜主要有微生物细胞体、代谢产生的胞外聚合物、腐蚀产物以及少量吸附的有机和无机物组成。Craig等[18]认为,细菌代谢产物的去极化包括H2S和FeS去极化。厌氧环境下,阴极产生H2S,从而使腐蚀加快,阳极反应也因FeS的生成而加快金属腐蚀。除了无机代谢物对腐蚀的影响,代谢产生的胞外聚合物在SRB腐蚀过程中也发挥重要作用。胞外聚合物是生物膜的主要组成成分,包括荚膜、粘液层、及其他表面物质,其有机部分主要由多聚糖、蛋白质和少量DNA、脂和腐植酸组成。刘宏芳研究团队[19]发现常压下培养14 d SRB产生的胞外聚合物量最多,而且低浓度的胞外聚合物 (EPS) 对碳钢具有抑制作用,而高浓度的对碳钢的腐蚀具有促进作用。Stadler等[20]发现SRB代谢产生的胞外聚合物可以明显的抑制碳钢的腐蚀,而且胞外聚合物的附着促进了更多SRB吸附于碳钢表面。Ghafari等[21]从底泥和温泉水中分离了21种细菌,研究发现仅有两种细菌产生的胞外聚合物对碳钢具有良好的缓蚀作用。由此可见,胞外聚合物与碳钢腐蚀之间的内在关系与微生物的浓度以及种类有着密切关系。然而,EPS引起的腐蚀机制仍然需要进一步系统研究。虽然有报道提出EPS中的某些组分具有较高的还原电位,具备一定的氧化能力,其自身的还原可以与阳极铁氧化构成电极对,从而加速试样的腐蚀过程,然而具体的活性物种尚不清楚[22]。Jin等[23]发现,适量的Fe浓度可以促进生物膜和EPS形成,而且EPS中部分官能团可以与铁离子结合,促进阳极溶解,进而加速腐蚀[22],该发现一定程度上为揭示EPS促进Fe的阳极溶解过程提供了理论支撑。
(3) 生物阴极催化 (生物电化学机理)。以上讨论的理论虽然在一定程度上解释了SRB的微生物腐蚀过程,但是并未明确SRB在腐蚀中所起的作用。随着研究的不断深入,人们慢慢发现了这些理论的局限性[24]。例如,Xu等[25]提出传统的阴极去极化理论并不能适用于所有SRB的腐蚀现象,有很多并不能分泌氢化酶的SRB仍然会对金属产生腐蚀。从微生物能量学的角度出发,维持SRB生命活动不仅消耗ATP,还需要电子[26]。他们基于“饥饿”实验,相比较于碳源 (电子供体) 充足的环境,在没有碳源或者很少量碳源存在的条件下,发生了更严重的微生物腐蚀[27]。基于此,他们认为SRB生物膜通过从基体金属材料中获取能量来获得维持其生命活动,提出了生物阴极催化硫酸盐还原机理 (BCSR)[28,29],如图1所示。BCSR理论认为在周围环境中有机碳源充足时,SRB首先利用有机物质作为电子供体。但是贴近金属表面的底层SRB生物被膜由于受到扩散和上层生物被膜消耗碳源的限制,导致其无法有效从外界获取碳源。为了获得维持其生存的能量,金属成为唯一电子供体[28],底层生物被膜从金属中捕获电子来进行厌氧呼吸、还原硫酸根,获取氧化还原过程中释放的能量,从而导致了严重的金属腐蚀[29]。文献[30,31]同样观察到长期处于无碳源环境下的SRB造成了更为严重的点蚀现象。生物阴极催化机制为微生物腐蚀研究提供了新的切入点,目前被认为是SRB促进金属局部腐蚀的主要原因之一。此外,BCSR理论的提出不仅清楚的阐释了硫酸盐还原菌腐蚀的具体过程,还解决了长期以来一直存在于微生物腐蚀领域中的一个问题:微生物为什么要腐蚀金属。BCSR理论还可以解释海洋环境下其它细菌对金属的腐蚀过程,如硝酸盐还原菌和古细菌同样是为了获得维持生存的能量而腐蚀金属[32]。
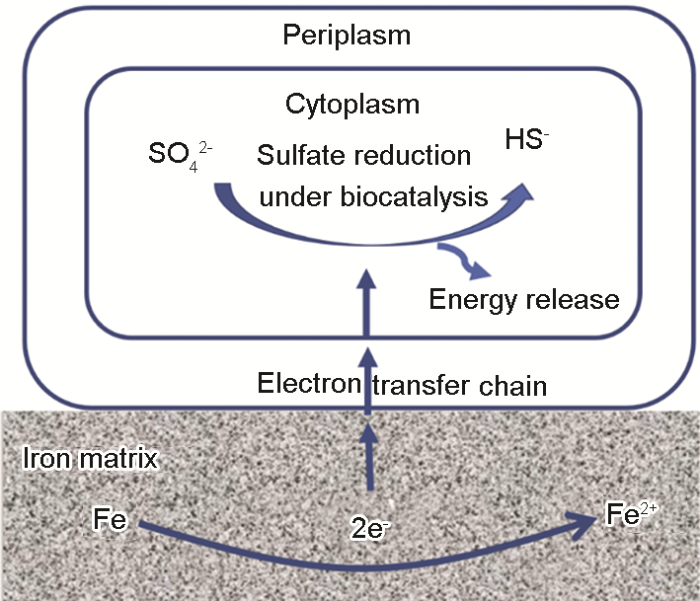
图1 生物阴极催化硫酸盐还原机理图[28,29]
进一步了解BCSR作用机理,生物膜的导电性以及细胞外的电子传递问题成为广泛关注的问题。Torres等[33]提出细胞外电子传递(EET) 的主要途径有直接电子传递与间接电子传递两种方式。直接电子传递主要依靠细菌细胞膜上的导电蛋白以及细菌自身与鞭毛类似的导电纳米线 (Pili)[34];而间接电子传递是通过细菌自身分泌的可溶性氧化还原分子进行电子传递。Xu和Gu[27]首次将胞外电子传递的概念引入到微生物腐蚀研究中,从生物电化学和生物能量学角度来解释微生物为什么以及如何造成金属腐蚀。图2描述了3种细胞外电子传递的方式,这3种传递方式并不是单一存在的,至于哪种传递方式发挥主导作用,要视具体微生物环境来定[16]。基因工程方法可抑制某些特定基因的蛋白和酶的表达,从而研究MIC中的电子传递载体,寻找抑制微生物腐蚀的靶点和方法,指导抗菌剂的研发、输油管道的材料选择以及抗菌材料的发展。然而海洋环境压力和温度的随机变化也有可能发生改变SRB代谢机制和对金属材料的腐蚀机制,目前尚缺乏相应的研究工作。
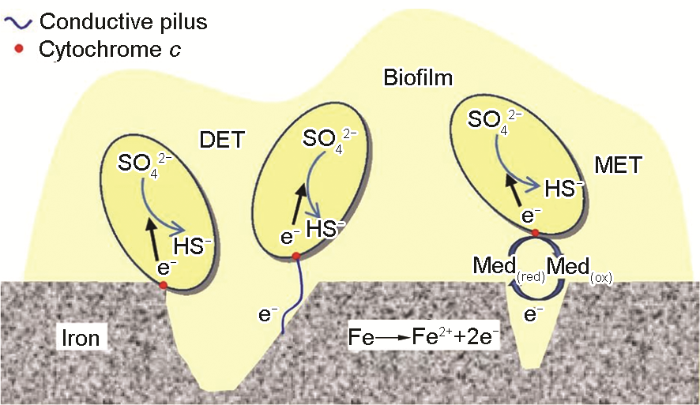
图2 SRB腐蚀金属过程中的电子转移方式[16]
2.1.2 好氧细菌腐蚀机制
IOB是一类以O2作为最终电子受体,通过氧化Fe2+至Fe3+获得能量生长的微生物,属于典型的好氧腐蚀菌[35]。除IOB外,铜绿假单胞菌也是一种能够引起碳钢腐蚀的常见好氧菌[12]。目前较普遍的观点认为典型的碳钢点蚀机理是由IOB腐蚀产物铁氧化合物引起的缝隙腐蚀[36]。例如,刘宏伟和刘宏芳[37]研究了IOB对Q235钢的腐蚀状况,结果表明,在空白无IOB存在条件下,试样腐蚀较轻且主要表现为均匀腐蚀,而在IOB存在的条件下,试样腐蚀加速且产生明显的点蚀坑。IOB对金属材料的整个腐蚀电化学过程中的化学反应式如下所示[38]:
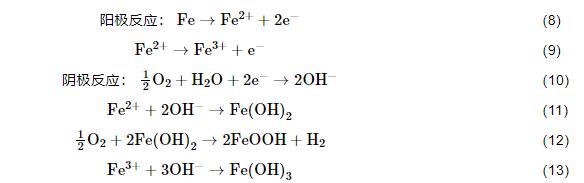
图3描述了由铁氧化合物引起的缝隙腐蚀机理图[36],好氧条件下,铁氧化合物膜下碳钢基底会形成很多小的阳极活性位点,阳极铁失去电子,阴极氧气被还原,氧的去极化过程会生产OH-,进而会产生铁氧化合物 (如FeOOH、Fe(OH)3等),铁氧化合物的形成又进一步促进阳极的溶解,从而会加速点蚀的形成。
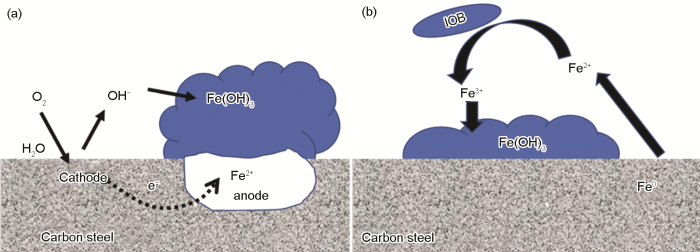
图3 由Fe(OH)3沉淀形成的点蚀机理和IOB缝隙腐蚀机理示意图[36]
2.1.3 混合细菌协同腐蚀
实际海洋环境复杂多变,种类繁多的微生物在海水中共同存在,它们彼此拮抗或促进,相比于单独存在的情况,微生物的代谢增殖特点必然会发生改变。在溶解氧丰富的海水区,好氧与厌氧菌之间的协同作用是造成金属腐蚀的一大主要关键因素。好氧微生物可改变环境参数,为厌氧菌的存活代谢提供局部厌氧环境。厌氧的SRB和好氧的IOB是目前公认的两大腐蚀性微生物,二者共同存在条件下的腐蚀行为和机理研究具有典型代表性,与实际情况更为相符。刘宏芳课题组[39]系统研究了在IOB与SRB共存条件下的碳钢腐蚀失效行为。研究认为,与单纯的SRB存在条件下相比较,混合菌共存产生更多含硫的腐蚀产物,说明IOB的存在促进SRB的生长与繁衍,导致更为严重的点蚀发生,腐蚀机理如图4所示。IOB与SRB首先附着在材料基底表面 (图4a);在有限的溶氧量条件下,IOB优先通过代谢增殖形成生物膜以及铁的氧化物沉积在材料基体表面,创建一个适合SRB存活的相对封闭的微环境,IOB消耗氧气的代谢活动为SRB的代谢繁殖所需的厌氧环境进一步优化了条件 (图4b)。除此之外,IOB的代谢产物铁氧化合物的沉积进一步巩固SRB生长所需的厌氧微环境并促进金属腐蚀的发生。生物膜的存在阻隔了SRB与外界碳源的接触,SRB直接从金属中获取电子维持生理活动所需的能量,最终导致点蚀的发生 (图4c)。总体来说,IOB与SRB的协同腐蚀的过程中,好氧菌首先为厌氧菌创造厌氧微环境并产生点蚀,继而厌氧菌进一步诱导并加剧腐蚀。这种协同作用可以能够合理地解释油田管线中混合细菌引起的局部穿孔现象。
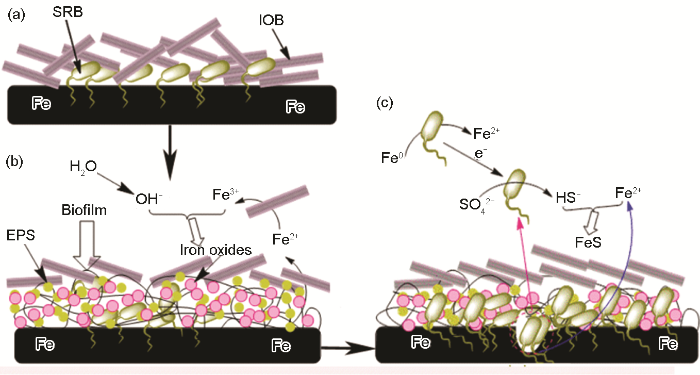
图4 SRB-IOB混合菌诱导金属点蚀机理示意图
2.2 应力腐蚀开裂
2.2.1 应力腐蚀开裂机理
临海管线面临着第二个典型的腐蚀问题为应力腐蚀 (SCC)。应力腐蚀开裂是一种比较严重的腐蚀形式,初级裂纹是在环境与应力协同作用下孕育形成,接着裂纹扩展并不断萌生次级裂纹,最终在没有明显的预兆下突然发生脆性断裂。海底油气集输管线在运行过程中必然承受着巨大的应力,从而造成应力腐蚀,应力腐蚀开裂是造成装备失效的主要原因之一,是油气输送管线运行过程中破坏性和危害性最大的一种腐蚀。应力腐蚀机理包括经典的阳极溶解机理与氢致开裂机理。传统的阳极溶解SCC机理,认为金属材料在应力和腐蚀的协同作用下,局部位置产生微裂纹,而裂纹尖端的快速阳极溶解引起应力腐蚀开裂[40]。氢致开裂理论则认为腐蚀开裂是在氢和应力的共同作用而导致金属材料产生脆性断裂,即氢脆。和常压环境相比,海洋环境中由于溶解氧浓度的减少,阴极反应会逐渐由吸氧反应向析氢反应转变,在金属表面发生阴极析氢反应,造成H在钢铁表面的吸附及向内部的扩散,由于氢原子很小,很容易在金属的晶格中移动,使钢铁结构脆变,同时在交变载荷作用下,钢铁结构很容易发生脆性断裂。同时,微生物诱导腐蚀也能产生氢源,促进金属氢致开裂的发生。另外一方面析氢反应产生的氢气由于气压的存在会进一步促进涂层的剥离[41]。
2.2.2 SRB诱导应力腐蚀开裂
现场失效分析表明,SRB的活动对基体材料应力腐蚀敏感性及应力腐蚀开裂均有一定的影响。在海底泥土中,SRB的存在对应力腐蚀开裂的影响表现为点蚀的发生。由于SRB会在碳钢表面形成疏松多孔的生物膜,生物膜中除了包含大量有毒的细菌代谢产物,还夹带H+、Cl-、H2S,均会在碳钢表面诱发并产生大量点蚀[42]。点蚀坑外加应力作用便能促进次生裂纹的产生及裂纹扩展,最终发生腐蚀开裂[43]。研究发现H2S分压增加会加速H原子在金属中的扩散,提高了金属发生氢致开裂的敏感性[44],另一方面,SRB存在下,使得局部环境呈现较低pH值,应力腐蚀开裂受阳极溶解和氢致开裂机理混合控制。文献[45]研究认为X80管线钢在应力腐蚀行为与SRB活性密切相关,一定含量的SRB可加速阳极溶解、硫化物的形成,与氢致开裂共同作用导致混合断裂。Biezma[46]研究认为SCC裂纹萌生和扩展速率取决于SRB的数量。Wu等[47]通过“有无加载应力和有无接种SRB”交互作用的实验观察到,加载应力与SRB的活动均可以改变生物膜特性,增大腐蚀敏感性,SRB诱导的点蚀是管线钢应力腐蚀开裂的直接原因。尽管大量研究已表明SRB对土壤环境、海洋环境中的钢结构材料的应力腐蚀表现出促进作用,然而SRB协同应力腐蚀的机理还尚且没有一个统一的定论,仍需要进一步研究。
2.3 缝隙腐蚀
临海管线面临着第三个关键腐蚀问题是临海管道裸漏后或补口损伤后,剥离涂层导致的缝隙腐蚀。沉积物覆盖导致的缝隙腐蚀是工业界非常常见的一种局部腐蚀,也是造成管线穿孔的主要原因之一。缝隙腐蚀包括孕育、开始和发展三个阶段,这三个阶段的发展速度又取决于缝隙的几何尺寸 (缝隙宽度、缝隙深度及缝隙内外面积比) 和环境条件 (溶解氧浓度、pH、Cl-浓度等)。缝隙腐蚀的机制主要包括氧浓差电池机制和IR降理论,这两种理论分别源于缝隙内外水化学特性的差异和缝隙内外的电位差。发生缝隙腐蚀的缝隙宽度在0.025~0.1 mm,该宽度足以使深海环境中高浓度Cl-进入并滞留在缝隙中,参与到缝隙内的腐蚀过程,促进局部腐蚀。氧浓差电池机制认为,在腐蚀孕育阶段,随着缝隙内金属的溶解,缝隙内O2被不断消耗,缝隙内正电荷增加,为了保持电中性,Cl-等进入缝隙内发生反应使溶液酸化,导致缝隙内溶液pH值降低而进一步加剧缝隙内金属溶解,上述过程反复进行最终造成严重的缝隙腐蚀。因此,氧浓差电池是此种机制下的腐蚀起因,而闭塞电池的酸化自催化作用则是造成缝隙腐蚀加速进行的根本原因。氧浓差电池机制是氧浓差与自催化效应共同作用下造成的缝隙腐蚀。IR降理论认为缝隙内O2被消耗殆尽后,缝内阳极区和缝隙外阴极区之间会出现很长的电流通路,若此通路流经的溶液介质电阻为R,当电流I流经此介质时会产生一个IR电压降,这个电压降导致缝隙内和缝隙外产生电位差,从而导致缝隙腐蚀发生[48,49]。此外,大小在1~2 μm的SRB同样可以进入缝隙,参与金属腐蚀。然而,目前SRB与缝隙腐蚀协同机制尚不清楚,需要开展针对性研究。涂层的剥离是一个缓慢生长的过程,深海环境中Cl-浓度较高,因此SRB、缝隙的几何尺寸和缝隙内水化学特性是影响剥离涂层下金属腐蚀的主要因素。在低温高压环境中,这些影响因素对于金属腐蚀发挥的关键作用需要进一步探明,对于剥离涂层下的金属管线与防护起到重要的作用。
3 临海环境腐蚀防护
海洋环境管线微生物腐蚀涉及材料与环境,因此,抑制和防止材料的微生物腐蚀就应该从这两个方面来着手。目前,海底管道一般采用涂层保护、阴极保护、或是使用防腐钢材和缓蚀剂杀菌剂的方式来进行微生物腐蚀的防护。
3.1 涂层保护
涂层保护是通过涂层的隔离作用来防止周围环境中的腐蚀介质进入,抑制电化学、化学反应,以达到防腐的目的。良好的表面和优质的涂层会显著提高深海装备的涂层保护效果,有效抑制深海装备的微生物腐蚀。涂层防护技术通常分内部防腐技术与外部防腐技术。
内部防腐技术主要针对管道内壁在油气运输过程中的内壁腐蚀的现象。为了防止管道内腐蚀,保障天然气管道的安全,目前常见的防腐材料是环氧有机物质 (包括熔结环氧粉末与液体环氧涂料),其具有抗化学腐蚀性强、抗氧化、耐磨等多种优势。
现阶段聚乙烯材料是石油管道防腐常用的一种管道外涂层防腐材料,这种材料在具体应用过程中的优势主要体现在涂层薄且附着力高、不透水、抗腐蚀、抗冲击性能强、无毒等,同时,这种材料也具有较高的经济性[50-52]。在一些管道规格变化较为频繁的输送管道施工中,常采用管道外壁缠绕聚乙烯材料的方式来对管道进行保护[53]。三层聚烯烃热缩节点涂层已经成为国内外普遍采用的节点补口涂层结构。此外,针对冷管弯道进行防腐处理,可采用外层烧结环氧粉末制成涂层,以增强管道的抗腐蚀性能。在压力较高的深海环境下,一般使用环氧沥青、喷塑、聚烯等涂层用于深海装备、管线防腐控制。
3.2 阴极保护
目前,大多数海洋设备都采用牺牲阳极的方法,其优点在于选材方便、安全可靠。这种方法的缺点是,海洋设备的防腐体系是处于一个动态的过程,阳极所能提供的保护电流及防腐涂层的状态在不同时期不能确切地得知,也不能实现自动控制,通常为了保证防腐效果,其阳极的数量要足够多。保护一旦停止,微生物附着引起的腐蚀将会对海下装备造成非常严重的后果。此外,海洋环境中的微生物对牺牲阳极本身也会产生不利影响,一些研究表明海水中的SRB能够直接或间接的促进牺牲阳极自身的溶解,从而减弱阴极保护效果。Liu等[13]研究了Al-Zn-In-Mg-Ti和Al-Zn-In-Sn两种铝基牺牲阳极在含SRB海泥中的腐蚀行为,实验结果表明,大量的SRB附着在铝基牺牲阳极表面,铝阳极在含SRB海泥中的腐蚀速率明显大于无菌海泥中的腐蚀速率且出现了更严重的点蚀。Guan等[54,55]研究了SRB诱导的Al-Zn-In-Cd牺牲阳极和5052铝合金的腐蚀机理,附着在铝合金表面的SRB能够改变金属材料和海水介质的界面特性,SRB参与电子传递过程并造成的阴极去极化效应加剧了铝基牺牲阳极的腐蚀,且其腐蚀产物在SRB的作用下从Al(OH)3和Al2O3转变为Al2S3和NaAlO2。因此,对于牺牲阳极的阴极保护而言,SRB能够促进牺牲阳极的腐蚀从而减少牺牲阳极的使用寿命,在阴极保护系统中间接地影响了海洋管道的腐蚀。海洋输油管道在服役期间还面临一些高温环境,在高温条件下铝合金牺牲阳极会出现电流效率降低,溶解不均匀等缺陷。在输油管线高温牺牲阳极中添加特定的稀土元素可以一定程度上解决牺牲阳极高温电化学性能下降的缺点[56]。一些研究表明在高温油气环境下,Al-Zn-ln-Sn-Mg阳极具有良好的电化学活性,相比Al-Zn-In-Cd阳极而言具有更负的开路电位和驱动电压[57]。外加电流阴极保护法是由外部直流电源直接向海洋设备上施加电流,使电子在金属表面富集,并通过控制海洋设备的电位使海洋材料发生阴极极化,从而达到降低或抑制海洋设备腐蚀的目的。海洋管道外加的电流阴极保护系统可随外界条件变化实现自动控制,使用周期更长。Guan等[58,59]研究了硫酸盐还原菌和阴极保护共存情况下的高强钢EQ70的腐蚀行为,结果表明,碳钢在-0.85 V (vs CSE) 的保护电位下其腐蚀速率大于无阴极保护状态,而在-1.05 V (vs CSE) 的状态下腐蚀速率减小,且腐蚀产物由硫化物转变为碳酸盐,该研究对SRB存在条件下的阴极保护应用有很强的指导意义。
3.3 防腐钢材与缓蚀剂杀菌剂
从材料角度出发,设计新型耐蚀材料可从本质上解决微生物的腐蚀问题。例如通过对材料表面进行合金化处理,对材料组织结构、力学性能实现优化,达到抗氢致开裂性能和耐微生物腐蚀性能的目的。通过在油气集输管道内壁加入缓蚀剂,可以有效降低内壁腐蚀问题的发生。加注缓蚀剂法是深海油气管道的一种重要防腐措施。常用的缓蚀剂主要是含氮有机物。通常是在可能会发生腐蚀的位置或管道重要位置使用缓蚀剂,在相应区域形成稳定的蚀剂膜 (保护膜),将化学腐蚀物质与内壁进行有效隔离,达到防腐的目的,更好地对油气集输管道进行保护,提高输油管道的运输能力。当前海洋管道缓蚀剂的使用主要是为了防止海洋管道停运封存期间的内腐蚀,海管停运封存期间管道内部会充满海水,微生物腐蚀会成为海管失效的重要原因。对于海洋管道腐蚀,目前已有各类绿色环保缓蚀剂的研究报道,钼酸盐类缓释剂[60]、L-精氨酸-Zn+体系[61]、N-酰基肌氨酸衍生物[62]、聚天冬氨酸[63]等绿色环保缓蚀剂在海水环境中均展现出良好的缓释效果,一些酶抑制剂还能够抑制微生物的附着进而减少腐蚀的发生[64]。此外,杀菌剂也是控制微生物腐蚀的常用方法,Wang等[65]研究认为,吡啶硫酮钠 (SPT) 不仅能够在低浓度下有效抑制硫酸盐还原菌的生长,而且SPT本身还具有明显的缓释效果,这种“一剂双功能”的效果显示出SPT优良的应用前景。
4 总结与展望
随着海洋经济的发展,微生物腐蚀导致的管线失效案例的增加,微生物对临海环境管道造成的腐蚀问题日益受到重视。因此对临海管道微生物腐蚀破坏行为、微生物腐蚀损伤机理及防护方法的研究将有利于全面了解海水管线的腐蚀情况,及时对管线腐蚀预警,避免发生更为严重的危害。目前虽然在微生物腐蚀规律方面做了大量研究,然而,实际海洋环境复杂多变,种类繁多的微生物在海水中共同存在,它们或彼此拮抗或彼此促进,相比于单独存在的情况,微生物的代谢增殖特点必然会发生改变,海底长距离油气集输管线微生物腐蚀控制仍然是国家能源安全、国民经济和社会发展的一个巨大挑战。目前大多数的研究还集中在实验室的研究,实验室模拟实验周期短,而微生物腐蚀是个长期的过程,因此要获得对工业生产具有指导性意义的数据,需要大量实验不断积累经验。此外,微生物的分布特征、腐蚀行为等因区域环境的差异而不同,导致微生物腐蚀规律复杂、腐蚀主要因素的分析与揭示仍是一大挑战。针对这方面问题,需要对海水区 (飞溅区、潮差区)、海泥区 (潮差带干湿交替区) 临海管道的运行环境,采用现场分离的微生物,采用模拟与加速试验方法,研究浪溅区、潮间带区、海泥区管线材料微生物腐蚀损伤机理,研究重要影响因素对临海管道微生物腐蚀的影响规律,建立微生物腐蚀模型及典型微生物腐蚀评价方法。
参考文献
1 Ma S D, Li W H, Sun H Y, et al. The biological control of ocean corrosion [J]. Total Corros. Control, 2006, 20(3): 5
1 马士德, 李伟华, 孙虎元等. 海洋腐蚀的生物控制 [J]. 全面腐蚀控制, 2006, 20(3): 5
2 Edyvean R G J. Biodeterioration problems of North Sea oil and gas production—A review [J]. Int. Biodeterior., 1987, 23: 199
3 Azis P K A, Al-Tisan I, Sasikumar N. Biofouling potential and environmental factors of seawater at a desalination plant intake [J]. Desalination, 2001, 135: 69
4 Yan T, Yan W, Dong Y, et al. Marine fouling of offshore installations in the northern Beibu Gulf of China [J]. Int. Biodeterior. Biodegrad., 2006, 58: 99
5 Heitz E, Flemming H C, Sand W. Microbially Influenced Corrosion of Materials [M]. Berlin: Springer-Verlag, 1996
6 Ma C, Chen C G, Jiang X B, et al. Distribution characteristics of marine bacteria in the China seas [J]. Med. J. Chin. PLA, 2012, 37: 909
6 马聪, 陈昌国, 蒋学兵等. 中国海域海洋细菌分布特征分析 [J]. 解放军医学杂志, 2012, 37: 909
7 Liu H W, Xu D K, Dao A Q, et al. Study of corrosion behavior and mechanism of carbon steel in the presence of Chlorella vulgaris [J]. Corros. Sci., 2015, 101: 84
8 Duan L N, Liu Q Y, Jia S J, et al. Microstructure characteristics and strength-toughness of X100 pipeline steel [J]. Chin. J. Mater. Res., 2012, 26: 443
8 段琳娜, 刘清友, 贾书君等. X100级管线钢的组织和强韧性 [J]. 材料研究学报, 2012, 26: 443
9 Dou W W, Jia R, Jin P, et al. Investigation of the mechanism and characteristics of copper corrosion by sulfate reducing bacteria [J]. Corros. Sci., 2018, 144: 237
10 Dong S, Bai X Q, Yuan C Q. Analysis of induced corrosion by fouling organisms on offshore platform and its research progress [J]. Mater. Prot., 2018, 51: 116
10 董硕, 白秀琴, 袁成清. 海洋平台污损生物诱导腐蚀分析及其研究进展 [J]. 材料保护, 2018, 51: 116
11 Zheng J Y. Influence of marine biofouling on corrosion behaviour [J]. J. Chin. Soc. Corros. Prot., 2010, 30: 171
11 郑纪勇. 海洋生物污损与材料腐蚀 [J]. 中国腐蚀与防护学报, 2010, 30: 171
12 Li H B, Zhou E Z, Ren Y B, et al. Investigation of microbiologically influenced corrosion of high nitrogen nickel-free stainless steel by Pseudomonas aeruginosa [J]. Corros. Sci., 2016, 111: 811
13 Liu F L, Zhang J, Sun C X, et al. The corrosion of two aluminium sacrificial anode alloys in SRB-containing sea mud [J]. Corros. Sci., 2014, 83: 375
14 Liu F L. Effect of sulphate reducing bacteria on corrosion of Zn, Al sacrificial anode materials in marine sediment [D]. Chongqing: Chongqing University, 2010
14 刘奉令. 海泥中硫酸盐还原菌对锌、铝牺牲阳极材料的腐蚀影响研究 [D]. 重庆: 重庆大学, 2010
15 Liu F L, Zhang S T, Zhang J, et al. Effects of SRB on corrosion of pure zinc anode in marine sediment [J]. Chin. J. Mater. Res., 2010, 24: 411
15 刘奉令, 张胜涛, 张杰等. 海泥中SRB对纯锌阳极腐蚀行为的影响 [J]. 材料研究学报, 2010, 24: 411
16 Li Y C, Xu D K, Chen C F, et al. Anaerobic microbiologically influenced corrosion mechanisms interpreted using bioenergetics and bioelectrochemistry: A review [J]. J. Mater. Sci. Technol., 2018, 34: 1713
17 Videla H A, Swords C, Edyvean R G J. Features of SRB-induced corrosion of carbon steel in marine environments [A].
17 Dean S, Delgadillo G, Bushman J. Marine Corrosion in Tropical Environments [M]. West Conshohocken, PA: ASTM International, 2000: 270
18 Craig B D, McNeil M B, Little B J. Discussion of “mackinawite formation during microbial corrosion” [J]. Corrosion, 1991, 47: 329
19 Liu H F, Liu T, Zheng B J, et al. Influence of EPS's activity on 13Cr stainless steel's pitting sensitivity [J]. J. Huazhong Univ. Sci. Techno. (Nat. Sci. Ed.), 2009, 37: 122
19 刘宏芳, 刘涛, 郑碧娟等. EPS活性对13Cr钢钝化膜点蚀敏感性的影响 [J]. 华中科技大学学报 (自然科学版), 2009, 37: 122
20 Stadler R, Wei L, Fürbeth W, et al. Influence of bacterial exopolymers on cell adhesion of Desulfovibrio vulgaris on high alloyed steel: Corrosion inhibition by extracellular polymeric substances (EPS) [J]. Mater. Corros., 2010, 61: 1008
21 Ghafari M D, Bahrami A, Rasooli I, et al. Bacterial exopolymeric inhibition of carbon steel corrosion [J]. Int. Biodeterior. Biodegrad., 2013, 80: 29
22 Chan K Y, Xu L C, Fang H P. Anaerobic electrochemical corrosion of mild steel in the presence of extracellular polymeric substances produced by a culture enriched in sulfate-reducing bacteria [J]. Environ. Sci. Technol., 2002, 36: 1720
23 Jin J T, Guan Y T. The mutual co-regulation of extracellular polymeric substances and iron ions in biocorrosion of cast iron pipes [J]. Bioresour. Technol., 2014, 169: 387
24 Xu D K, Li Y C, Gu T Y. Mechanistic modeling of biocorrosion caused by biofilms of sulfate reducing bacteria and acid producing bacteria [J]. Bioelectrochemistry, 2016, 110: 52
25 Xu D K, Li Y C, Song F M, et al. Laboratory investigation of microbiologically influenced corrosion of C1018 carbon steel by nitrate reducing bacterium Bacillus licheniformis [J]. Corros. Sci., 2013, 77: 385
26 Gu T Y, Jia R, Unsal T, et al. Toward a better understanding of microbiologically influenced corrosion caused by sulfate reducing bacteria [J]. J. Mater. Sci. Technol., 2019, 35: 631
27 Xu D K, Gu T Y. Carbon source starvation triggered more aggressive corrosion against carbon steel by the Desulfovibrio vulgaris biofilm [J]. Int. Biodeterior. Biodegrad., 2014, 91: 74
28 Zhang P Y, Xu D K, Li Y C, et al. Electron mediators accelerate the microbiologically influenced corrosion of 304 stainless steel by the Desulfovibrio vulgaris biofilm [J]. Bioelectrochemistry, 2015, 101: 14
29 Gu T Y. New Understandings of biocorrosion mechanisms and their classifications [J]. J. Microb. Biochem. Technol., 2012, 4: 1
30 Jia R, Tan J L, Jin P, et al. Effects of biogenic H2S on the microbiologically influenced corrosion of C1018 carbon steel by sulfate reducing Desulfovibrio vulgaris biofilm [J]. Corros. Sci., 2018, 130: 1
31 Chen Y J, Howdyshell R, Howdyshell S, et al. Characterizing pitting corrosion caused by a long-term starving sulfate-reducing bacterium surviving on carbon steel and effects of surface roughness [J]. Corrosion, 2014, 70: 767
32 Liu H W, Xu D K, Wu Y N, et al. Research progress in corrosion of steels induced by sulfate reducing bacteria [J]. Corros. Sci. Prot. Technol., 2015, 27: 409
32 刘宏伟, 徐大可, 吴亚楠等. 微生物生物膜下的钢铁材料腐蚀研究进展 [J]. 腐蚀科学与防护技术, 2015, 27: 409
33 Torres C I, Marcus A K, Lee H S, et al. A kinetic perspective on extracellular electron transfer by anode-respiring bacteria [J]. FEMS Microbiol. Rev., 2010, 34: 3
34 Reguera G, McCarthy K D, Mehta T, et al. Extracellular electron transfer via microbial nanowires [J]. Nature, 2005, 435: 1098
35 Liu H W, Gu T Y, Asif M, et al. The corrosion behavior and mechanism of carbon steel induced by extracellular polymeric substances of iron-oxidizing bacteria [J]. Corros. Sci., 2017, 114: 102
36 Wang H, Ju L K, Castaneda H, et al. Corrosion of carbon steel C1010 in the presence of iron oxidizing bacteria Acidithiobacillus ferrooxidans [J]. Corros. Sci., 2014, 89: 250
37 Liu H W, Liu H F. Research progress of corrosion of steels induced by iron oxidizing bacteria [J]. J. Chin. Soc. Corros. Prot., 2017, 37: 195
37 刘宏伟, 刘宏芳. 铁氧化菌引起的钢铁材料腐蚀研究进展 [J]. 中国腐蚀与防护学报, 2017, 37: 195
38 Liu H W, Gu T Y, Zhang G A, et al. The effect of magneticfield on biomineralization and corrosion behavior of carbon steel induced by iron-oxidizing bacteria [J]. Corros. Sci., 2016, 102: 93
39 Liu H W, Fu C Y, Gu T Y, et al. Corrosion behavior of carbon steel in the presence of sulfate reducing bacteria and iron oxidizing bacteria cultured in oilfield produced water [J]. Corros. Sci., 2015, 100: 484
40 Hehemann R F. Stress corrosion cracking of stainless steels [J]. Metall. Trans., 1985, 16A: 1909
41 Xiong F P, Wang J L, Ahmed A F, et al. Research progress of sulfate-reducing bacteria induced SCC [J]. Corros. Sci. Prot. Technol., 2018, 30: 213
41 熊福平, 王军磊, Ahmed A F等. 硫酸盐还原菌诱导应力腐蚀开裂研究进展 [J]. 腐蚀科学与防护技术, 2018, 30: 213
42 Liu Q, Li Z, Liu Z Y, et al. Effects of H2S/HS- on stress corrosion cracking behavior of X100 pipeline steel under simulated sulfate-reducing bacteria metabolite conditions [J]. J. Mater. Eng. Perform., 2017, 26: 2763
43 Li X, Xie F, Wang D, et al. Effect of residual and external stress on corrosion behaviour of X80 pipeline steel in sulphate-reducing bacteria environment [J]. Eng. Fail. Anal., 2018, 91: 275
44 Zhou C S, Zheng S Q, Chen C F, et al. The effect of the partial pressure of H2S on the permeation of hydrogen in low carbon pipeline steel [J]. Corros. Sci., 2013, 67: 184
45 Xie F, Li X, Wang D, et al. Synergistic effect of sulphate-reducing bacteria and external tensile stress on the corrosion behaviour of X80 pipeline steel in neutral soil environment [J]. Eng. Fail. Anal., 2018, 91: 382
46 Biezma M V. The role of hydrogen in microbiologically influenced corrosion and stress corrosion cracking [J]. Int. J. Hydrogen Energy, 2001, 26: 515
47 Wu T Q, Xu J, Sun C, et al. Microbiological corrosion of pipeline steel under yield stress in soil environment [J]. Corros. Sci., 2014, 88: 291
48 Kennell G F, Evitts R W, Heppner K L. A critical crevice solution and IR drop crevice corrosion model [J]. Corros. Sci., 2008, 50: 1716
49 Laycock N J, Stewart J, Newman R C. The initiation of crevice corrosion in stainless steels [J]. Corros. Sci., 1997, 39: 1791
50 He T, Jańczewski D, Jana S, et al. Efficient and robust coatings using poly (2-methyl-2-oxazoline) and its copolymers for marine and bacterial fouling prevention [J]. J. Polym. Sci., 2016, 54A: 275
51 Banerjee I, Pangule R C, Kane R S. Antifouling coatings: recent developments in the design of surfaces that prevent fouling by proteins, bacteria, and marine organisms [J]. Adv. Mater., 2011, 23: 690
52 Liu J H, Qian S Q. Marine bioadhesion and defenses [J]. Corros. Prot., 2010, 31: 78
52 刘继华, 钱士强. 海洋生物附着及其防护技术 [J]. 腐蚀与防护, 2010, 31: 78
53 Selim M S, Shenashen M A, El-Safty S A, et al. Recent progress in marine foul-release polymeric nanocomposite coatings [J]. Prog. Mater. Sci., 2017, 87: 1
54 Guan F, Zhai X F, Duan J Z, et al. Influence of sulfate-reducing bacteria on the corrosion behavior of 5052 aluminum alloy [J]. Surf. Coat. Technol., 2017, 316: 171
55 Guan F, Duan J, Zhai X, et al. Interaction between sulfate-reducing bacteria and aluminum alloys-Corrosion mechanisms of 5052 and Al-Zn-In-Cd aluminum alloys [J]. J. Mater. Sci. Technol., 2020, 36: 55
56 Liao H X, Qi G T, Yu K X. Research on sacrificing anode of high-temperature Al alloy containing rare earth and application [J]. Corros. Prot. Petrochem. Ind., 2004, 21(4): 19
56 廖海星, 齐公台, 喻克雄. 含稀土高温铝合金牺牲阳极的研究与应用 [J]. 石油化工腐蚀与防护, 2004, 21(4): 19
57 Sun Y L, Wang N, Zhou Y, et al. Electrochemical performance evaluation of high temperature sacrificial anode under well environment [J]. Hot Work. Technol., 2017, 46(14): 99
57 孙雨来, 王楠, 周勇等. 油井环境中高温牺牲阳极的电化学性能评价 [J]. 热加工工艺, 2017, 46(14): 99
58 Guan F, Zhai X F, Duan J Z, et al. Influence of sulfate-reducing bacteria on the corrosion behavior of high strength steel EQ70 under cathodic polarization [J]. PLoS One, 2016, 11: e0162315
59 Guan F, Zhai X F, Duan J Z, et al. Progress on influence of cathodic polarization on sulfate-reducing bacteria induced corrosion [J]. J. Chin. Soc. Corros. Prot., 2018, 38: 1
59 管方, 翟晓凡, 段继周等. 阴极极化对硫酸盐还原菌腐蚀影响的研究进展 [J]. 中国腐蚀与防护学报, 2018, 38: 1
60 Wei Y L, Tian Y Q, Wang Y H, et al. Study on corrosion inhibition of compound corrosion inhibitor of molybdate in seawater [J]. Adv. Mater. Res., 2012, 581/582: 755
61 Gowri S, Sathiyabama J, Rajendran S. Corrosion inhibition effect of carbon steel in sea water by L-arginine-Zn2+ system [J]. Int. J. Chem. Eng., 2014, 2014: 607209
62 Kaskah S E, Pfeiffer M, Klock H, et al. Surface protection of low carbon steel with N-acyl sarcosine derivatives as green corrosion inhibitors [J]. Surf. Interfaces, 2017, 9: 70
63 Ma X M, Qian B, Zhang J, et al. The inhibition effect of polyaspartic acid and its mixed inhibitor on mild steel corrosion in seawater wet/dry cyclic conditions [J]. Int. J. Electrochem. Sci., 2016, 11: 3024
64 Liu F, Zhang L, Yan X, et al. Effect of diesel on corrosion inhibitors and application of bio-enzyme corrosion inhibitors in the laboratory cooling water system [J]. Corros. Sci., 2015, 93: 293
65 Wang J L, Hou B S, Xiang J, et al. The performance and mechanism of bifunctional biocide sodium pyrithione against sulfate reducing bacteria in X80 carbon steel corrosion [J]. Corros. Sci., 2019, 150: 296
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





