摘要
介绍了Ti及其合金发生氢脆可能的深地质环境因素,分别论述了H在Ti中扩散,Ti发生氢脆的实质及机理,总结了多种钛合金的临界氢浓度,分析了深地质环境下Ti储罐发生氢脆的可能性。最后对研究Ti储罐在深地质环境中氢脆问题进行了展望。
关键词: 高放核废料; Ti; 氢吸收; 氢脆; TiHx
核能由于其低成本、高效性以及不会产生温室气体等优势,已经被广泛应用于包括医学、国防、农业和工业等领域,极大地改善了人类的生活。然而,高放射性核废料是核能利用过程中不可避免产生的废物,具有强放射性、较长的半衰期、毒性大等特点,其所含的多种高放射性元素对人体及生物圈的危害极大。例如,锝 (Tc) 是裂变产物,因为其半衰期长、裂变率高和高锝酸盐的环境迁移率,使得核废料的长期处置变得更为复杂[1]。目前各国都在大力发展核电站,核电快速发展必然会产生更多的高放射性核废料。就我国而言,预计到2030年,将产生3000 m2高放射性核废料。因此,世界各国已将高效处理高放射性核废料视为核能工业发展所面临的重要挑战[2]。
关于高放射性核废料处置方案,研究人员曾提出“深海床处置”、“冰冻处置”、“液压笼处置”、“太空处置”及“深地质处置”等[3-8]。目前各国普遍接受的方案是深地质处置法,即将高放射性核废料处置在距离地表约为500至1000 m深的合适岩体中的储库里,形成了以固化后的高放射性核废料、外包装材料 (金属储罐) 和缓冲回填材料组成的工程屏障和围岩及其周围的地质环境构成天然屏障的“多屏障系统”[9-11]。金属储罐作为核废料的第一道屏障尤为重要,Ti及其合金由于良好的耐蚀性,是储罐备选材料之一。加拿大和日本将Ti及其合金作为储罐备选材料,并开展了大量研究[12,13]。目前美国计划在尤卡山的镍合金容器上使用钛防滴罩[14-18]。
Ti及其合金良好的耐蚀性归根结底是因为其表面形成稳定的氧化膜。有研究[19]表明,即使是微量的氧也可以防止Ti上H+发生还原反应,除非它与更活泼的金属相结合。Ti及其合金表面氧化膜比较完整也会对氢向材料内部渗透产生阻碍。Qin等[20]研究了H在TiO2中的扩散模型,结果表明H在TiO2中扩散系数要比H在Ti中小3个数量级。但是氧化膜十分薄,通常只有几纳米。也有研究[21]表明,在没有氧化膜的Ti表面上会发生H的快速吸收。然而如果Ti表面氧化膜不能保持完整,其在无氧环境下十分脆弱,尤其是高温环境下[22,23]。如果暴露在含氢环境中,Ti极易吸收氢。Dwivedi和Vishwakarma[24]将Ti归类为易受氢脆影响的材料。目前,国内对Ti储罐在深地质处置过程中可能发生氢脆的研究近乎没有。然而,全面理解其可能发生氢脆的机理对预测Ti储罐寿命以及开发新型钛合金十分必要。本文介绍了Ti及其合金发生氢脆可能的深地质环境因素,分别论述了H在Ti中扩散,Ti发生氢脆的实质以及机理,总结了多种钛合金的临界氢浓度,分析了深地质环境下Ti储罐发生氢脆的可能性。最后对研究Ti储罐在深地质环境中氢脆问题进行了展望。
1 深地质近域环境
众所周知,金属材料腐蚀行为与其周围环境密切相关,因此开展核废料储罐在近域环境中的腐蚀行为是十分必要的。核废料储罐需要在深地质下埋藏数万年甚至是数十万年,其近域环境也会随着时间不断演变,目前多以模型为主模拟演变规律。核废料储罐近域环境条件主要包括以下几个方面:
(1) 温度。温度的变化主要是由高放射性核废料所含的放射性核素衰变而产生的衰变热引起,其主要通过辐射、对流以及传导等方式从废物体向外传递[25]。黄彦良等[26]预测了核废料储罐近域环境中温度、湿度的长期演变规律 (见图1),表明我国高放核废料在深地质处置过程中储罐近域温度最低约在22 ℃;而在埋藏十年后达到最高,约为90 ℃。
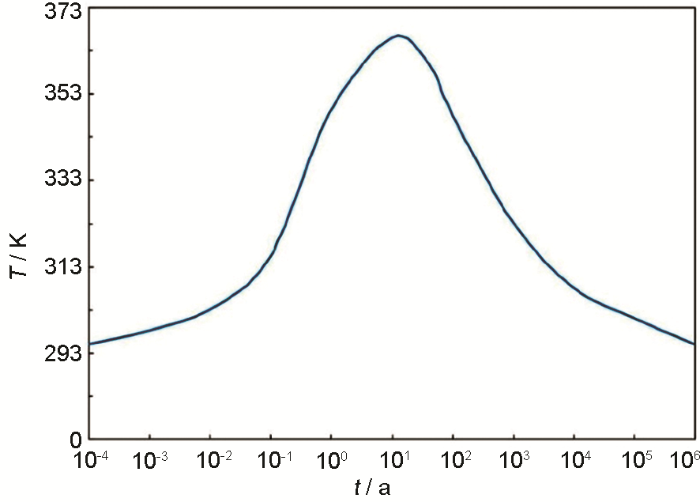
图1 模拟我国核废料储罐表面温度的演变[26]
(2) 地下水成分。甘肃北山作为我国高放射性核废料储库的预选区,其地下水有3种类型:盆地孔隙-裂隙水,水富集最丰富的沟谷洼地孔隙-裂隙水以及分布最广的山地基岩裂隙水[27]。黄彦良等[28]总结表明,北山地区地下水为偏碱性的高矿化咸水,阳离子主要包括Na+,K+,Ca2+以及Mg2+,阴离子主要为HCO3-,Cl-,SO42-以及NO3-。值得关注的是其中Na+,Cl-和SO42-含量最高,且比含量普遍较低的K+和NO3-高出近4倍。
(3) 溶解氧含量。Yang等[29]通过求解水生物地球化学耦合模型模拟了缓冲材料孔隙中的耗氧过程,获得了不同模拟情景下的O2浓度变化;并显示在储存库封闭后,最快约4 a后,O2几乎耗尽。其氧浓度变化如图2所示。
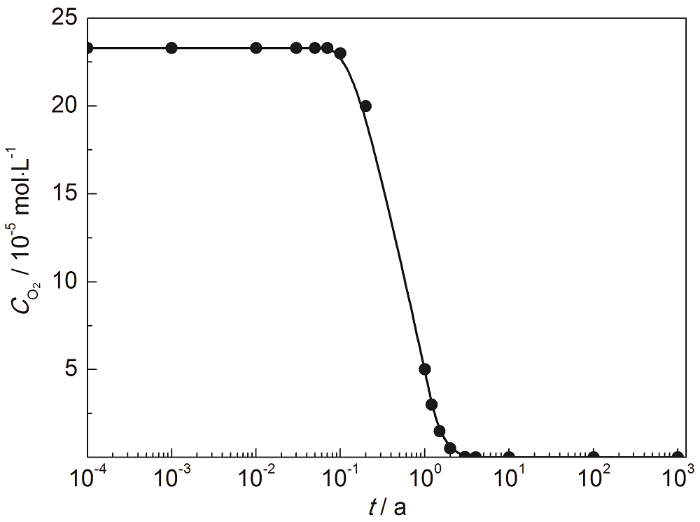
图2 深地质环境中氧浓度的模拟演化
(4) 辐射剂量。高放射性核废料中的主要辐射源是锕系元素的衰变 (例如U,Np,Pu等) 以及β衰变 (例如137Cs和90Sr)。由于来源于寿命较短的裂变产物,β衰变将会成为核废料储罐储存前500年的主要辐射源。有研究依据玻璃化的固体废料、储罐容器、空间布置以及厚度的不同,根据模型预测在高放核废料处置后,其储罐容器外表面的初始照射剂量率约为0.2~2 Gy·h-1,并且在100 a后降低一个数量级[30-32]。
Schutz[33]认为,导致钛合金发生氢脆的主要因素有3个:(1) Ti表面有一种不断生成新原子氢的机制 (如腐蚀);(2) 当反应温度高于80 ℃时,氢扩散到α-Ti中的速率更为明显;(3) pH低于3或高于12,或施加的电位大于-0.70 V (相对于SCE)。综上所述,我国深地质环境满足了Ti作为核废料储罐发生氢脆的条件。
2 Ti及其合金吸氢与氢脆
2.1 H在Ti及钛合金中的扩散
在研究Ti发生氢脆行为之前,首先需要清楚H在Ti中的扩散。在早期Wasilewski和Kehl[34]测得H在α-Ti中的扩散系数为:
![]()
式中,R为热力学常数,T为温度,Dα单位为cm2·s-1。
而Papazoglou和Hepworth[35]给出的扩散系数方程为:
![]()
可见,lnDα与1/T呈线性关系。然而这两组数据的差异是因为不同的实验方法导致的。Wasilewski和Kehl利用H的β相稳定作用在α-Ti膜上形成β-Ti表面层。这个被H饱和的表面层会成为内部α相的恒定氢源。而Papazoglou和Hepworth在足够低的压力下将H2直接从气相引入到α相中以防止β相的形成。以上两种H在纯钛中的扩散系数均在温度高于400 ℃条件下测得。虽然通过外推法能够得到低温下的扩散系数,有研究[36]表明这种方法获得的低温下的氢扩散系数并不是十分可靠。Wipf等[37]的研究也表明,H在Ti中的扩散在低温时存在隧道扩散。Phillips等[38]根据Ti表面生成的TiHx厚度随充氢时间变化关系测得了低温下 (25~100) ℃ H在Ti中扩散系数,方程如下:
![]()
这种根据氢化物厚度求得扩散系数的过程较为复杂,不仅需要通过表征方法确定TiHx具体成分,氢化物厚度测量也比较困难。Zhang等[39]通过改良的Devanathan-Stachurski电解池测得了低温 (25~100) ℃下H在纯Ti中的表观扩散系数。由于H在Ti中扩散极其缓慢,通过使用超薄的钛片大大缩短了测量时间,测量结果如下:
![]()
该法所得扩散系数小于前3种方法测定的结果,说明该测定结果是H在Ti中的表观扩散系数,该法适合应用于多种环境介质中的测量,能够直观反映H在该环境中的扩散快慢。
Bustard等[40]通过核磁共振法测定γ相TiHx中的氢扩散机理。根据自旋晶格弛豫时间T1的测量结果,可以确定原子跳跃τd之间的平均逗留时间。这两个量与跳跃长度L和示踪相关因子fT有关:
![]()
最终测得氢在TiH1.55和TiH1.71中的扩散系数方程式为:
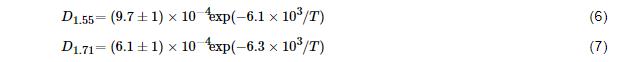
可见,其指前因子比值9.7/6.1=1.59,这与空位浓度的比值1.55很好地吻合。Stalinski等[41]指出,在γ相TiHx中,指前因子和空位浓度 (2-x) 之间存在直接的比例关系。
比较以上结果可知,H在TiHx中扩散系数小于在Ti基体中的扩散系数,这证实了TiHx的形成会阻碍H继续向Ti中扩散。这个结果与H在Ti中表观扩散系数最小相符合。
Christ等[42]采用电化学方法对试样充氢得到不同氢浓度分布,最后根据数值模拟计算了H在3种不同的钛合金中的扩散系数。结果同样显示,H在钛合金中的扩散系数与样品中氢浓度无关并遵循Arrhenius方程。并且认为在α钛合金中氢扩散最慢,而在稳定的β钛合金中最快,这种差异在低温下最显著,随着温度的升高而降低。Miyoshi等[43]研究了H在Ti,Ti88Al12以及Ti3Al中的扩散,认为随着Al含量的增加,扩散系数的指前因子和活化能增加。Johnson和Nelson[44]通过使用质谱仪的方法,采用气态氢,H从空心圆柱试样内表面壁进入并从外表面渗出,测得了温度400~800 ℃,H2压力在0.533~266.644 Pa条件下渗透的H2流量P (单位:mol·Pa·s-1·cm-2),其方程为:
![]()
其中,H2压力为p,渗透活化能为6.23×10-5 J·mol-1。
H在金属中的扩散行为取决于许多因素。对于多晶结构的纯金属,这些因素包括晶体结构的类型、晶界、内应力和空位浓度。在工程合金中,氢扩散受其它因素的影响,如合金元素、杂质的类型和含量、多种相存在等。此外,真实的微观结构大部分可以充当氢陷阱。因此,通过实验测定H在复杂的工业合金上的扩散系数,以及相应的频率因子和微观结构特征的活化能是非常困难的,并且需要对微观机理和过程进行详细了解。另一方面,由于H在Ti中扩散十分缓慢,也加大了测定难度。这也是现有关于H在钛中扩散研究较少的原因。
2.2 Ti及其合金氢脆
Ti及其合金发生氢脆的实质是因为在其吸收一定量的H之后会与其反应生成TiHx,而TiHx十分容易脆化。TiHx是一种灰色粉末,在空气中稳定,这种氢化物在约1000 ℃时可完全脱氢。因此,有必要全面了解TiHx的性质。
2.2.1 TiHx的性质
如果氢吸收达到临界水平 (室温下H在α-Ti中的溶解度在1.64~12.27 mg/cm3之间),Ti表面就会形成氢化物,氢化物的脆性和弹性性质与母体晶格有很大的不同[45-48]。Ti是副族元素,其核外d轨道存在2个电子空位,扩散在其中的原子氢的核外电子易进入d轨道,钛氢化合物的标准生成Gibbs焓变值偏负,从热力学角度来说也是很容易生成的。
TiHx中的H与Ti的原子比例 (H/Ti) 与氢原子的扩散通量有关,因此不同实验条件下得到的TiHx不一定相同。Yan等[49]计算得到其平均原子比例 (H/Ti) 接近1.6~1.8之间 (除了最低充氢电流密度0.5 mA·cm-2)。Millenbach和Givon[50]通过X射线衍射法测得更高电流密度下 (5~20 mA·cm-2),原子比例 (H/Ti) 在1.62~1.78之间。然而,Phillips等[51]计算出在外加充氢电流密度0.05~3.0 mA·cm-2下氢化物中的H/Ti从1.2增加到1.5 (在0.05 mol·L-1 H2SO4溶液中)。Zhang等[39]分别在外加电流密度1 mA·cm-2的0.05 mol·L-1 H2SO4溶液和模拟北山地下水溶液中进行充氢,X射线衍射测定H/Ti为1.5。
根据钛-氢相图 (图3)[52],更容易理解TiHx的结构。γ-氢化物具有相对于钛原子的fcc晶胞,氢原子随机分布在四面体间隙位置 (CaF2型结构)。对于接近极限成分H/Ti为2的高氢浓度,氢化物在较低温度下转变为四方结构;在较低浓度区,H在α相中的固态溶解度在室温下较小,所以氢化物经常出现在纯Ti中[53]。
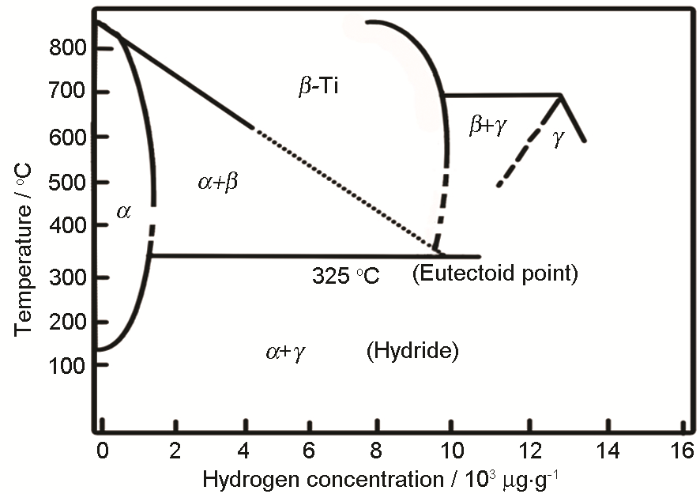
图3 钛-氢相图[52]
Numakura和Koiwa[53]研究表明,在低温40~60 ℃下的钛合金中,TiHx可以形成3种不同的晶体结构和形貌,这取决于TiHx中H/Ti的不同值:具有低氢浓度 (TiH0~1.5) 的氢化物 (有序的fcc结构);具有中等氢浓度 (TiH1.5~1.9) 的氢化物 (fcc结构);具有高氢浓度 (TiH1.9~2.0) 的氢化物 (fcc结构)。Panin等[54]认为TiH2具有fcc结构,Ti处在结点位置,每个晶胞有4个Ti原子,H原子位于fcc的四面体间隙位置,每个晶胞有8个H,即CaF2结构,此fcc氢化物的点阵常数a约为0.44 nm,比hcp结构α-Ti的点阵常数 (0.2953 nm) 要大得多。在可测量反应速度的足够高温下,钛-氢合金仅在与气态氢处于平衡状态下存在,此时H2压力是金属中氢浓度和温度的函数[55]。根据TiH1.75~TiH1.93之间的氢化物离解热,可以推算出如下关系:
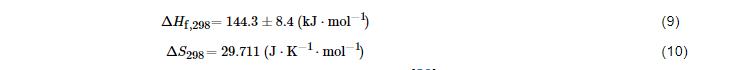
由于钛-氢相图的复杂性,其不同温度区域的热力学性质可能还存在一些新的特性[56],仍需深入研究。
Setoyama等[57]研究了TiHx的力学性能,结果表明TiHx的晶格参数随氢含量增加而线性增加。TiHx的纵向和剪切声速均小于钛基体的。TiHx的弹性模量和显微硬度也比钛基体的小,并且都与氢含量有关,其中显微硬度随着H的加入而降低。Xu等[58]采用纳米压痕技术也测定了TiHx的硬度、弹性模量和屈服应力等力学性能。通过电沉积法得到TiHx,经扫描电子显微镜和X射线衍射证实该TiHx为TiH1.971,然而其结果与Setoyama等[57]的结果相反,TiHx的硬度、弹性模量和屈服应力都稍高于纯Ti的。
关于TiHx的热力学性质,有研究[59]表明TiHx的Debye温度比纯钛的小,并且随着氢含量的增加而降低。TiHx的热容大于钛基体的热容,这是由于氢化物的振动导致的。而纯Ti和TiHx的热导率几乎相同[59]。Setoyama等[57]由声速和晶格参数估算的TiHx的Debye温度小于纯Ti的,这与热容量测量的Debye温度一致。Ito等[60]不仅研究了TiHx热力学性质,同时还对电学性质进行了研究。结果同样显示,氢化物的热导率与钛基体的热导率相同,但会随温度的升高略有增加,电子和声子在TiHx的热导率中起着重要的作用。TiHx的导电性略低于Ti金属的,且与氢含量几乎无关,表现出类似金属的温度依赖性。氢化物的电导率随氢含量的变化未发生明显的变化。Ti-H体系的Seebeck系数因氢化而由正变为负,TiHx的绝对值保持在最低值,这是金属材料的典型特征。与此同时,TiHx热稳定性极高。王耀奇等[61]研究了TiHx的动态分解,认为TiHx的热分解开始温度为510 ℃,热分解过程由4个阶段构成,不同阶段的热分解机制不同,速率控制步骤也不同,反应过程中生成了TiHx (0.7<x<1.1) 中间产物,其热稳定性高于TiH2。
总而言之,关于TiHx中H/Ti值在不同环境中是否发生变化还有待进一步研究,最终可以根据H/Ti值去估算Ti中氢含量。关于TiHx的力学性能目前还存在一些争议,因此仍需深入研究。
2.2.2 Ti及其合金氢脆机理
(1) 纯Ti。目前对纯Ti氢脆的研究较少,主要因为细晶粒的纯Ti试样以低至中等应变率进行拉伸实验时,具有很强的抗氢脆性能。Wang等[45]研究了纯Ti在pH为1的6% (质量分数) NaCl溶液中,温度在70 ℃条件下的氢脆行为。结果表明,Gr-2纯Ti氢脆敏感性较低,而Gr-3纯Ti在低于-800 mV (vs SCE) 时较敏感,并在Gr-3纯Ti内部观察到氢化物相,而Gr-2纯Ti内部未观察到,这主要是因为Gr-3纯Ti中氧浓度较高造成的。Briant等[62]也认为仅仅在纯Ti表面形成一定厚度的TiHx并不会影响其力学性能。然而在高温下,纯Ti暴露在氢气中时,很容易形成TiHx同时变得非常脆,与此同时随着氢浓度的增加,材料的断裂应变减小,屈服强度和极限抗拉强度都增加。通过扫描电子显微镜可观察到H对纯Ti断裂表面的影响,当氢含量增加时,断裂表面从未充氢材料中的大微孔聚结转变为小微孔 (含有600 μg/g H的试样),最后转变为脆性面 (含有3490 μg/g H的试样)。Yan等[49]则认为氢化物完全覆盖在纯Ti表面时,会抑制H进一步向钛基体中的扩散。这与上述讨论H在TiHx中扩散速率较慢相一致。Nishimura等[63]采用恒载法研究了工业纯Ti在硫酸和盐酸溶液中的氢致开裂随外加应力和实验温度的变化规律。结果表明,纯Ti在盐酸溶液中的氢脆敏感性小于在硫酸溶液中的,并推测这是由于裂纹尖端形成的TiCl3的抑制作用所致。研究[64]纯Ti在局部氟化物溶液中的应力腐蚀开裂结果显示,冷轧试样在含氟溶液中暴露5 d后出现窄裂纹,裂纹与分枝有关,这是应力腐蚀裂纹的特征。暴露在氟化物溶液中的冷轧试样显示出脆性断裂。相反,未暴露试样的断裂方式具有韧性,局部氟溶液可引起工业纯Ti的应力腐蚀开裂。(2) 钛合金。当钛合金在室温下暴露于外部氢环境中时,从微观角度看来,主要包含α相的钛合金在气-金属界面处或靠近界面处,脆性氢化物相重复形成和断裂而降解[65]。当只有α相存在时,降解对外部氢的压力不敏感,因为α相的氢化物几乎可以在任何合理的氢分压下形成。Shih等[46]则认为对于hcp结构的含有4% (质量分数) Al的α钛合金,在室温下暴露于气态氢环境中,根据应力强度的不同,可产生两种断裂机制。在低应力下,氢化物的反复形成和解理断裂使裂纹扩展;在高应力强度下,裂纹扩展速率超过氢化物在裂纹前形成的速率时断裂模式转变,氢化物增强的局部化塑性是产生裂纹的主要机制。由于β钛合金具有很高的氢溶解度,并且不易形成氢化物,因此被普遍认为氢脆敏感性较低 (除高氢压力外)[66]。然而Young和Scully[67]观察到Ti-Mo-Nb-Al在远远低于氢化β相所需的氢浓度下发生了氢脆。此外,由于H是一种很强的β稳定剂,这些β合金中的α相在高温下暴露于氢中时可以转变为β相。因此,由于存在细小的沉淀,针状α相是大多数β合金的主要强化机制,它们的强度会随着高温下氢的吸收而降低[68]。研究人员[69,70]先后研究了镍钛超弹性合金在含0.1% (体积分数) 盐酸的甲醇溶液中吸氢引起的拉伸强度下降以及加工硬化镍钛合金在酸性氟化磷酸盐 (APF) 溶液中的氢脆行为。都是将其浸泡在溶液一段时间后测试其抗拉强度,同时利用热脱附分析测定钛合金中吸氢量。结果表明,由于试样横截面外围形成脆性层,断裂模式由韧性变为脆性。吸附氢的量随浸泡时间呈线性增加。对于加工硬化镍钛合金,当吸氢量大于500 μg/g时,材料的力学性能下降;而镍钛超弹性合金在吸氢量为50~500 μg/g之间时,其拉伸强度已经下降。因此,加工硬化的镍钛合金对氢脆的敏感性较低。Yokoyama等[71,72]研究了Ti-0.2%Pd合金在氟化物溶液中的吸氢性能以及应力拉伸断裂。结果表明,Pd能够很好抑制H在Ti中的吸收,然而Ti-0.2%Pd合金的断裂敏感性却高于工业纯Ti的。
总结以上研究可见,纯Ti表面形成的氢化物对其力学性能影响不大,只有当氢化物分布均匀才会发生明显影响作用。然而,氢化物的生成对氢吸收有阻碍这一点对纯Ti抗氢脆性能有利。同时个别离子的存在也对其氢脆有影响。然而对于钛合金而言,因为合金中的多种元素的影响,其氢脆机理较为复杂。
3 深地质环境中钛储罐发生氢脆可能性
根据之前所讨论的金属储罐与缓冲回填材料界面O2含量演变规律可见,在放置完储罐封闭地下储库后,储库会逐渐从一个有氧的环境转变为无氧的环境,更有利于析氢反应的发生。析氢反应有几个基本步骤[73],反应式如下:
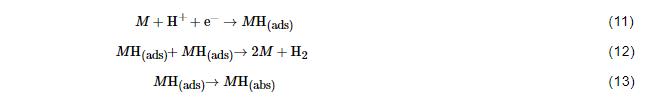
其中,式 (11) 为H的吸附,式 (12) 为和H重组形成H2分子,式 (13) 为一些吸附的H原子可能被吸收到晶格中。
Ti储罐在吸氢后材料自身的性能可能发生改变,同时储罐在服役期间会受到热-水-力的耦合作用,还可能遭受地震等强地壳运动的破坏,产生前期难以预见的氢诱导脆裂。因此,Ti储罐所处的深地质近域环境更为苛刻复杂。
3.1 氢来源
根据Shoesmith等[74]的观点,主要有两种产氢来源,一种是地下水受到高放核废料辐照分解所产生的H,另一种是电化学腐蚀所析出的H原子。然而有研究[74]表明,除了在高剂量率 (>102 Gy·h-1) 和高温 (>150 °C) 条件之外,放射性产生的H的直接吸收似乎并不显著。因此,大多数研究多以钛储罐在深地质环境中的电化学腐蚀产H为主。电化学腐蚀所产生的H又根据腐蚀类型分为以下3种[75]:
(1) 全面腐蚀产H。反应方程式为:
![]()
氢吸收速率将由腐蚀反应速率控制,腐蚀反应速率决定可吸收氢的生成速率。由于TiO2极不溶解,所以腐蚀反应将有效地限制在氧化膜的生长反应中。
(2) 缝隙腐蚀产H。反应方程式为:
![]()
一旦发生缝隙腐蚀,由缝隙外的钝化表面上的氧还原和缝隙内的质子还原来支持,从而导致足够数量的原子氢吸收,最终大量氢化物形成。由于氢吸收需要通过氧化膜 (TiO2),因此吸收过程中必然经历氧化膜的氧化还原转变:
![]()
缝隙腐蚀产氢与钛材料本身关系密切,例如Gr-2钛合金,较容易发生缝隙腐蚀,然而对于Gr-7和Gr-16钛合金,几乎不会发生缝隙腐蚀。
(3) 钛合金与其它金属电耦合产H。Ti与活性金属 (如Zn、Mg、Al和碳钢) 的耦合作用已被充分证明,当温度超过80 ℃时,有可能导致氢吸收和最终脆化[33]。
3.2 临界氢浓度
H在Ti中的来源大体包括两种:内氢和外氢[76]。内氢,即H在钛材使用之前就存在于金属内部。一般是由于材料在冶炼、热加工、热处理、酸洗、电镀、焊接、冷加工等工艺过程中吸收的H。外氢是指材料在使用过程中从外界环境中进入的H[52]。因为H在Ti中有一定的固溶度,该固溶度存在最大临界值,当Ti中的氢含量超过了H在Ti中的固溶度时,就与Ti结合生成TiHx。而临界氢浓度 (HC) 和H在Ti中的固溶度完全不同。
HC是一个阈值,当Ti中氢浓度超过这一临界值时,就只有快速裂纹扩展而不再观察到慢速裂纹扩展。在临界氢浓度下,裂纹扩展不是不可避免的,但一旦达到或超过临界值,就可能出现快速失效。因此,临界氢浓度可被视为定义材料对氢脆敏感性的特性[75]。然而不同的钛合金,其临界氢浓度也不尽相同。Hardie和Ouyang[77]采用慢应变速率技术对预裂纹的致密拉伸试样进行预充氢处理,认为当合金中氢含量超过200 μg/g时,Gr-5钛合金的断裂韧性就发生显著变化。Clarke等[78]认为,Gr-2和Gr-12钛合金的HC均随温度显著升高,在92~100 ℃的温度范围内达到约1000 μg/g。Sorensen等[79]认为,在出现任何可测量的塑性损失之前,Gr-12钛合金的氢含量大于500 μg/g,而前提条件是β相的出现和制造织构等其他因素基本保持不变。HC取决于材料的强度。Ikeda和Quinn[80]研究结果表明,Gr-16钛合金的HC值在1000~2000 μg/g范围。而根据Gr-7和Gr-16钛合金的相似性和Pd的作用,估测Gr-7钛合金的HC至少为1000 μg/g[75]。
在临界氢浓度的基础上,Ti储罐中的氢含量可以作为评估其在服役期是否发生氢脆的标准。因此,测定Ti储罐氢含量尤为重要。尽管H的定量分析方法众多,主要包括真空熔融法、气相色谱法、定容测压法、气体容量法、质谱分析法、库仑定氢法等,现代定氢仪普遍采用惰性气体熔融法和惰性气体加热提取法来测定氢含量[81]。然而Ti储罐要在深地质环境中埋藏数万年甚至数十万年,对其进行实验测定显然不现实。目前的研究多以建立模型去估算Ti储罐中的氢含量。根据恒定的薄膜生长速率和腐蚀速率,Shoesmith等[74]推导出,对于全面腐蚀的Ti储罐,H的浓度可根据以下表达式计算:
![]()
式中,HA是氢含量 (g·mm-3),ρTi为钛密度 (4.50 g·cm-3),fh是氢吸收效率,Ruc为全面腐蚀速率 (mm·a-1),t为钛储罐处置时间 (a),MTi为钛原子质量 (47.9 g·mol-1),do为金属厚度的一半。由该式可知Ti储罐腐蚀速率和其氢吸收效率是估算氢含量的关键。Hua等[75]根据通过失重法测得的Gr-7钛合金腐蚀速率,以及Okada[82]测得硫酸条件下H在Ti中的吸收效率 (0.005~0.015),根据式 (17) 求得在1×104 a以内,氢含量低于Gr-7钛合金的HC (1×103 μg·g-1)[75],因此得出结论由全面腐蚀而吸收的氢不足以使Gr-7钛合金在处置1×104 a间发生氢脆。国内并未有从事氢脆的学者对Ti储罐在深地质环境中发生氢脆做出评价。Zhang等[83,84]分别估测了Gr-2和Gr-16钛合金在模拟地下水及高压实膨润土环境下的腐蚀速率随地质处置年代的变化。
总结以上研究可见,Ti储罐中氢含量的测量是预测其发生氢脆可能性的关键,然而氢含量只能进行估测,并且取决于氢吸收效率及腐蚀速率。关于Ti储罐深地质环境下腐蚀行为研究较多,但是有关氢吸收效率研究甚少。必须说明,Okada[82]所研究的Ti中氢吸收效率并不是在深地质环境条件下获得的。
4 结束语
综上所述,Ti及钛合金作为高放核废料储罐在深地质环境中服役期间有发生氢脆的可能,其发生氢脆的实质是材料吸氢后所产生脆性的氢化物,然而因为不同钛合金中的合金元素不相同,因此具体发生氢脆的机理也不尽相同。关于Ti储罐的氢脆研究还存在以下难点需要研究和探讨:
(1) 目前对Ti储罐发生氢脆的评估主要建立在氢含量的预测上,然而现有研究对其预测并不准确,需要研究更好的方法去估算钛储罐在深地质环境中埋藏至数万年累积的氢含量。
(2) Ti储罐在深地质环境下 (尤其在缓冲材料膨润土环境下) 的腐蚀过程中的渗氢效率目前尚不清楚。
(3) 高放核废料的辐射性对Ti储罐氢脆的影响研究甚少,可通过辐照对Ti储罐腐蚀行为的影响去判断对其氢脆的影响。
(4) 可以进一步开发和优选合金元素,设计具有较大临界氢浓度的钛合金。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





